Pasamos una parte muy importante de nuestras vidas durmiendo, pero en el caso de los niños esto puede suponer más de la mitad del día.
La primera descripción del síndrome SOAS en los niños fue realizada por Willian Hill en 1889, si bien hay autores, que posiblemente desconocedores de la comunicación de Hill, mencionan a Osler en 1892 como quien lo describió en primer lugar.
Hasta hace poco tiempo a este síndrome no se le ha dado en los niños la misma importancia que se le daba en los adultos. Actualmente se ha comprobado que es una patología frecuente entre los niños y que produce una morbilidad significativa. En 1976 Guilleminault presentó la primera serie importante de casos y en 1981 Brouillette publicó el primer estudio controlado del síndrome.
El SOAS infantil difiere del adulto tanto en su etiología como en sus manifestaciones clínicas, diagnóstico y tratamiento. La American Thoracic Society lo define como un trastorno respiratorio durante el sueño caracterizado por una situación de obstrucción parcial prolongada de la vía aérea, o bien una situación de obstrucción completa intermitente, que en ambos casos altera la ventilación normal durante el sueño y los patrones del mismo.
Se han de diferenciar la apnea obstructiva del recién nacido y del lactante de la del resto de la infancia. Las entidades nosológicas dentro de las roncopatías en el niños son las mismas que en el adulto: roncopatía simple, síndrome de resistencia aumentada de las VAS y SAOS.
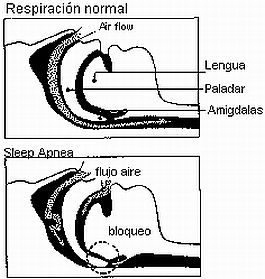 FISIOPATOLOGÍA.
FISIOPATOLOGÍA. En el capítulo 4 se ha expuesto la fisiopatología del síndrome en el adulto.
En la infancia esta fisiopatología tiene algunos aspectos peculiares a tener en cuenta:
- A diferencia del adulto, el niño presenta durante el sueño una disminución de la frecuencia respiratoria.
- Como en el adulto, durante el sueño se reduce la capacidad residual funcional y se duplica, o aumenta, la resistencia de la VAS al paso del aíre. Recuérdese lo que ocurre durante el sueño REM: la respiración se vuelve errática con variaciones importantes de la frecuencia respiratoria y del volumen corriente, pueden aparecer apneas centrales y hay una marcada disminución del tono muscular de los músculos intercostales y de todos los de las VAS. Pues bien, los niños duermen proporcionalmente más sueño REM que los adultos y los problemas respiratorios están mucho más ceñidos a esta fase del sueño que en los adultos. No obstante el número de despertares aurosales secundarios a esta causa es menor que el del adulto.
- La hipofaringe del niño es fácilmente colapsable. Su presión de cierre es muy cercana a la atmosférica, por lo que una vez cerrada, se requiere más fuerza para abrirla. Para mantenerla abierta es necesario un adecuado tono muscular en la zona. El sito de obstrucción más habitual es la base de la lengua por desplazamiento posterior de la base de la misma contra la hipofaringe.
- Los niños pequeños tienen una pared torácica con una distensibilidad mucho mayor que la de los adultos. En lactantes, la distensibilidad torácica es hasta tres veces mayor que la pulmonar, lo que provoca movimientos torácicos abdominales paradójicos durante la inspiración, esto aumenta el trabajo respiratorio, fundamentalmente durante la fase REM cuando la actividad de los músculos intercostales está disminuida. La distensibilidad torácica es igual a la pulmonar a los dos años de edad. Los niños con obstrucción de la vía aérea tienen más respiración paradójica durante el sueño que los adultos.
- Los niños tienen también una menor respuesta a la hipoxia durante el sueño. Esta respuesta es bifásica; así, aunque de manera inicial se produce un aumento de la ventilación, en un segundo tiempo aparece un descenso de la frecuencia respiratoria que puede conducir a la apnea. Cualquier grado de hipoxia nocturna es perjudicial para el niño, ya que está en pleno desarrollo neuropsicológico y el cerebro del niño es más sensible a la hipoxia que el del adulto, por lo que en general se aconseja tratar a los niños que presenten alteraciones oximétricas durante el estudio de sueño, aunque no tengan sintomatología diurna.
- Por lo que respecta a la hipercapnia la respuesta a la misma en el niño, en condiciones normales, es similar a la del adulto. Ahora bien, está comprobado que en niños con SAOS el umbral de respuesta a la hipercapnia está aumentado.
- Las apneas centrales en las que no se detectan movimientos respiratorios pueden ser de hasta 20 segundos de duración y son relativamente frecuentes en niños, siendo su significación clínica muy dudosa. Las desaturaciones transitorias asociadas a una apnea central o a respiraciones periódicas son frecuentes en los niños sanos, fundamentalmente en los lactantes.
ETIOLOGÍA EN EL NEONATO Y LACTANTE.
El SAOS en el neonato, en la mayoría de los casos, comienza por presentar un problema de diferenciación entre apnea obstructiva y apnea central, lo que a veces no es sencillo y más teniendo en cuenta que algunos casos pueden asociarse ambas formas.
- Apneas centrales. Como se informó en el capítulo introducción son aquellas que no están relacionadas con el esfuerzo respiratorio. El neonato tiene un desarrollo neurológico incompleto, por lo que las irregularidades respiratorias se pueden presentar sin una causa etiológica conocida con más frecuencia que en el adulto y esto se pone más frecuentemente de manifiesto en los prematuros que pueden presentar en los primeros meses de vida apneas centrales, que poco a poco van disminuyendo en frecuencia e intensidad hasta desaparecer: apnea de la premadurez o apnea del lactante. Para que estas apneas puedan ser consideradas como patológicas han de tener una duración superior a 15 seg., y son claramente patológicas por encima de 20 seg. Otras causas de apneas centrales son: alteraciones cardíacas, hematológicas, algunas enfermedades víricas, alteraciones metabólicas, neurológicas (convulsiones), pulmonares y neuromusculares. Estas apneas ponen en peligro la vida del niño.
- Apneas obstructivas: se consideran patológicas, como en el adulto, las superiores a los 10 seg. Las causas pueden ser muy variadas. Algunas son muy graves, de modo que si no se actúa inmediatamente producen la muerte del recién nacido: atresia laríngea o traqueal, membranas o causas de compresión externa como un bocio. La atresia de coanas y la laringomalacia son las causas más frecuentes. Trastornos neurológicos productores de parálisis de cuerdas vocales e incordinación en la musculatura respiratoria. En los primeros días de vida se ha de valorar las causas nasales de obstrucción entre ellas la rinitis supurada del lactante. En los lactantes de meses la causa más frecuente, como ocurre ya en el resto de la infancia, es la hipertrofia adenoamigdalar.
- Apnea mixta: la obstrucción de las VAS, si bien lo más normal es que produzca apneas obstructivas, también puede producirlas centrales por inhibición refleja del esfuerzo respiratoria y por hipoxemia. El reflujo gastroesofágico es otra causa de apneas mixtas pues puede causar obstrucción de la faringe por el material ácido y apneas centrales por reflejo vagal o coincidiendo con alteraciones del SNC.
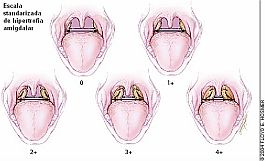 ETIOLOGÍA EN LA INFANCIA.
ETIOLOGÍA EN LA INFANCIA. La obstrucción nasal por la causa que fuere, puede ser origen de esta patología al igual que en el adulto: desviación septal, RA, poliposis, etc.
Los trastorno neuromusculares pueden presentarse al igual que en los lactantes.
La causa más frecuente es la hipertrofia adenoamigdalar, lo que no quiere decir que sea la única, de hecho se pueden encontrar síntomas de SAOS en niños sin hipertrofia del anillo de Waldeyer. El diámetro anteroposterior de la faringe es proporcionalmente más pequeño en el niño que en el adulto. Se ha demostrado que más importante que la hipertrofia en sí, es la relación entre el tamaño del tejido linfoide y la vía aérea, que va cambiando según el niño va creciendo, y los factores dinámicos que condicionan la correcta función de los músculos de la faringe. Hay que tener en cuenta que muchos niños con importante hipertrofia adenoamigdalar no tienen alteraciones respiratorias durante el sueño, mientras que otros con una hipertrofia amigdalar discreta si tienen problemas importantes.
El paladar blando en el niño no es causa de obstrucción, pues está poco desarrollado.
Los tumores de la cavidad oral o la nasofaringe actúan de misma forma que la hipertrofia adenoamigdalina.
Las malformaciones craneofaciales, como en los síndromes de Apert, Crouzon y Treacher Collins. También los niños con síndrome de Down suelen padecer estadísticamente con mayor frecuencia apneas pues suelen tener hipoplasia mandibular inferior, macroglosia, disminución del espacio faringe. Los niños acondroplásicos suelen presentar obstrucción y apnea de sueño. Se calcula que el 30-45% de los pacientes con síndrome de Down padecen SAOS, incluso aunque no exista sospecha clínica.
Incluso sin tener una malformación determinada como las mencionadas, los niños con la barbilla pequeña y triangular, retrognatia, facies larga y estrecha, paladar ojival o paladar blando alargado, presentan con mayor frecuencia alteraciones respiratorias durante el sueño.
La obesidad puede ser un factor predisponente para el SAOS en los niños, sobre todo en los adolescentes, aunque esta asociación no es tan frecuente como en la edad adulta. Al contrario, frecuentemente los niños con SAOS tienen retraso del desarrollo ponderal.
 EPIDEMIOLOGÍA.
EPIDEMIOLOGÍA. El síntoma principal del SAOS infantil es el ronquido. Se calcula que entre el 7-9% de los niños ronca regularmente; sin embargo, en la mayoría de los casos este ronquido no se asocia con sintomatología de SAOS nocturna ni diurna, tratándose solamente de ronquido primario o roncopatía simple.
Se estima que la prevalencia del verdadero SAOS en la infancia está entre el 0,7% y el 3%.
Puede aparecer a cualquier edad, aunque el pico de máxima incidencia está entre los 3 y los 5 años de edad, coincidiendo con el momento en que la relación tamaño de tejido adenoideo/tamaño de tejido de la faringe es más desfavorable.
No existe ningún predominio según sexo.
DIAGNÓSTICO.
Se va a basar en la clínica. Se han de diferenciar los procesos graves que pueden poner en peligro la vida del niño, de los procesos banales que muchas veces curan espontáneamente con el crecimiento.
Los síntomas fundamentales durante el sueño son la tríada clásica:
- Ronquido.
- Dificultas respiratoria.
- Alteración del patrón normal del sueño que se acompaña de movimientos y posibilidad de despertares frecuentes.
El interrogatorio con los padres ha de ser muy detallado en busca de síntomas asociados a los referidos y que pueden reforzar la sospecha clínica. Es importante establecer las diferencias de si existe o no obstrucción, si se trata de un cuadro de apnea o convulsiones y diferenciar ronquido de estridor. Los padres a menudo hablan de ronquido, pero a veces no se han fijado si presentan paradas respiratorias; evidentemente, este último síntoma está ligado al grado de observación de los padres, pues en ocasiones no sólo refieren el ronquido y las apneas, sino también hipersomnia diurna, atragantamiento y respiración bucal. Es típico del niño que los síntomas empeoren durante las infecciones respiratorias como las amigdalitis, con mejoría cuando ceden estos cuadros intercurrentes.
El cuadro puede ser referido y presentado como un problema respiratorio. Los cuadros de aparición inmediata tras el parto sugieren un trastorno congénito como la atresia coanal. Cuando se presentan a los tres o cuatro meses se ha de pensar en una laringomalacia, aumentando la sintomatología en posición prona y con el llanto. La parición brusca del cuadro sugiere un cuerpo extraño. La dificultad respiratoria durante la alimentación es posible que se deba a una fístula tráqueo-esofágica. El desarrollo gradual del cuadro indica un problema tumoral, estenosis subglótica o papilomas.
Entre los 3 y 7 años de edad es la hipertrofia adenoamigdalar la causa más frecuente.
Los síntomas nocturnos incluyen, como en el adulto, el aumento del esfuerzo respiratorio, sueño intranquilo, sudoración, apneas observadas por los padres, incluso cianosis.
Durante el día la mayoría de los niños están asintomáticos y su exploración física puede ser normal. Solo los casos más graves presentan respiración diurna bucal, respiración ruidosa, disminución del rendimiento, problemas de comportamiento, hipersomnia, hipertensión sistémica, insuficiencia cardíaca, retraso del desarrollo psicomotor o falta de crecimiento. Pero a diferencia del adulto no existe una relación entre los síntomas diurnos del SAOS y la posibilidad de desarrollar complicaciones más serias. Existen pacientes con retrasos importantes del crecimiento, retraso del desarrollo, e incluso con cor pulmonale como síntoma de presentación sin tener prácticamente síntomas diurnos.
Al igual que en el adulto el diagnostico comienza con una sospecha clínica razonable, siendo la polisomnografia el método de evaluación y confirmación diagnóstica. La aportación de un fragmento de video domestico durante el sueño puede ser una prueba de valor diagnóstico muy práctica y fácil de realizar. Las indicaciones para realizar una polisomnografía en el niño son las siguientes:
- Para la diferenciación entre ronquido primario y SAOS.
- Presentación de respiración dificultosa durante el sueño con pausas o respiración paradójica, observados por personal sanitaria, documentada con vídeo, etc.
- Aparición de posibles complicaciones del SAOS, sin otra explicación posible: somnolencia diurna, patrones de sueño alterados, policitemia, hipertensión pulmonar, enlentecimiento del crecimiento, etc.
- Niños con factores de riesgo posquirúrgico: menores de dos años, SAOS grave, presencia de enfermedades neuromusculares o de la línea media.
- Patologías con factores de riesgo: drepanocitosis con crisis veno-oclusivas nocturnas, laringomalacia, obesidad, broncodisplasia.
- Control evolutivo en niños con CEPAP, con persistencia de síntomas.
Como ocurre con los adultos, no existen criterios definidos para su valoración, se considera patológica la aparición de un índice de apnea/hipopnea mayor de 3 y se considera significativa toda caída en la saturación del 3-4%. Al igual que en los adulto pueden realizarse los otros niveles de exploración polisomnográfica.
Con respecto a las pruebas complementarias, las técnicas a realizar son las mismas que en el adulto, si bien cave destacar que en los lactantes no existe consenso sobre cuales son los estándares definitivos.
El éxito del tratamiento puede depender de que los criterios utilizados para el diagnóstico tengan en cuenta las posibles comorbilidades asociadas, o no, a la hipertrofia adenoamigdalar.
DIAGNÓSTICO DIFERENCIAL.
Se ha de diferencia con otras patologías respiratorias que igualmente pueden producir hipoventilación durante el sueño, pero cuya causa no es obstructiva.
- Síndromes de hipoventilación central: consiste en la aparición de incremento de los niveles de pCO² en sangre secundario a un fallo en la estimulación de la ventilación a nivel del sistema nervioso central, en ausencia de una alteración pulmonar primaria o disfunción de musculatura respiratoria. Auque la hipercapnia e hipoxemia secundaria a la hipoventilación que aparece en estos síndromes, es más grave durante el sueño, también puede aparecer durante el día. Estos síndromes pueden ser congénitos como son el síndrome de hipoventilación central congénito (síndrome de Ondine) y el síndrome de hipoventilación central de instauración tardía. Igualmente pueden ser secundarios o asociados a alteraciones neurológicas o malformaciones como el mielomeningocele, hidrocefalia, Arnold-Chiari, etc
- Patología crónica pulmonar durante el sueño: puede aparecer en diferentes enfermedades pulmonares crónicas como la enfermedad obstructiva pulmonar, las deformidades de la pared torácica y enfermedades neuromusculares (distrofia miotónica).
TRATAMIENTO.
En el lactante el tratamiento unas veces tiene una finalidad vital y en otras preventiva o curativa de situaciones patológicas que, a la larga, pueden ocasionar complicaciones graves y a menudo irreversibles, como hipertensión pulmonar a cor pulmonale.
Al igual que en el adulto, para que el tratamiento sea correcto es fundamental que el diagnóstico de la causa productora de la apnea esté previamente bien identificada. Pero en el niño el tratamiento no debe de basarse en controlar los síntomas diurnos como en los adultos, sino más importante es evitar las complicaciones a largo plazo.
Fármacos: las metilxantinas (teofilinas o cafeínas) son útiles en lactantes con apneas de premadurez.
El CPAP resulta útil en algunos lactantes y niños cuando no es posible la cirugía o hay recurrencias de los síntomas tras la misma, pero sólo puede utilizarse en medio hospitalario.
Adenomigdalectomia. La hipertrofia denoamigdalar asociada a SOAS demostrado es una indicación absoluta de adenoamigdalectomía. La adenoamigdalectomía es el tratamiento de elección tradicional cuando la hipertrofia del tejido linfoide es la causa de la obstrucción y con este tratamiento se alcanzan unas tasas de curación del 80%. Algunos de estos casos son pacientes de alto riesgo al asociar malformaciones o patología cardiopulmonar que exigirá un postoperatorio inmediato muy controlado. El 20% de los fracasos quirúrgicos son niños con otra comorbilidad asociada: los dos factores más importantes son la obesidad y la severidad del SOAS, siendo menos frecuentes el reflujo gastroesofágico, las alteraciones anatómicas, etc. En estos casos de riesgo se debe de valorar la conveniencia de realizar tras la cirugía un control/seguimiento polisomnográfico que puede indicar la necesidad de tratamiento adicional. En la adolescencia puede producirse una reproducción del cuadro, después de un tratamiento exitosos con la Adenomaigdalectomia en la infancia, especialmente en los casos de riesgo como son los SOAS más severos, los casos con alteraciones craneoencefálicas o neuromusculares o cuando se desarrolla obesidad.
Los casos con malformaciones craneofaciales, parálisis cerebral o hipotonía muscular el tratamiento es mucho más complejo, requiriendo una aproximación multidisciplinar.
La uvulopalatofaringoplastia es excepcional tener que practicarla en el niño, pero en niños con úvulas excesivamente grandes puede ser necesaria. Parece ser útil en niños con parálisis cerebral.
La oxigenoterapía nocturna puede ser útil en determinados casos, aunque no se recomienda su utilización generalizada, pues no mejora el trabajo respiratorio ni la sintomatología diurna, además puede provocar un empeoramiento en la ventilación e incluso retrasar el tratamiento quirúrgico definitivo.
COMPLICACIONES.
La complicación más grave en el niño es el fallo ventricular derecho seguido de cor pulmonale e hipoventilación alveolar. Hoy es raro llegar a esta situación que requiere un tratamiento sin dilación. La posibilidad de esta situación puede darse en niños con síndrome de Down en los que pueden asociarse cardiopatías congénitas a SAOS producidas por hipertrofia adenoamigdalar y macroglosia.
Retrasos del crecimiento: el cuadro de SAOS se relaciona con un descenso en la producción de hormona del crecimiento, que parece secundario a la desestructuración del sueño, y, sobre todo, a la pérdida de sus fases profundas. En estos retrasos puede influir también la disminución de apetito e ingesta, un mayor gasto calórico y la hipoxemia.
La limitación crónica del flujo aéreo nasal puede desarrollar anomalías morfológicas craneomandibulares. La hipertrofia adenoamigdalar puede producir una insuficiencia respiratoria nasal que condicionará el crecimiento facial pudiendo ser un factor que predispone a la roncopatía crónica en el futuro. Estas anomalías, en si mismas, pueden alterar la estabilidad de las vías respiratorias altas. En este sentido, el tratamiento temprano de los trastornos obstructivos de las VAS en la infancia pueden prevenir el eventual desarrollo de un SAOS en el adulto.
A medio plazo en la esfera psicointelectual, pueden aparecer alteraciones del comportamiento que pueden afectar a la relación social del niño, insuficiente desarrollo de las capacidades cognitivas. Se ha demostrado la existencia de una relación entre las apneas de sueño y la hiperexcitabilidad en niños, pudiendo constituir un factor desencadenante o agravante de la misma. Al mismo tiempo se ha observado que el síndrome de piernas inquietas en los niños podría constituir una primera manifestación de esa hiperexcitabilidad.
Descargar tema completo 
 FISIOPATOLOGÍA.
FISIOPATOLOGÍA. ETIOLOGÍA EN LA INFANCIA.
ETIOLOGÍA EN LA INFANCIA. EPIDEMIOLOGÍA.
EPIDEMIOLOGÍA.