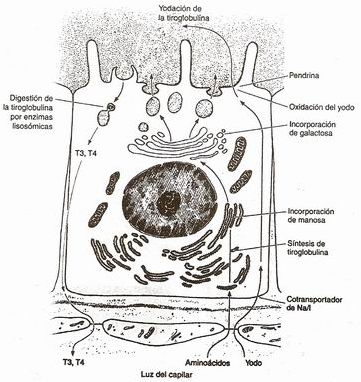
EL FOLÍCULO.
EL FOLÍCULO. La glándula está compuesta por unas unidades estructurales-funcionales con forma esféricas llamadas folículos tiroideos con forma de sacos o acinis, cuyas paredes están recubiertas por una monocapa de cc cuboidales, llamados tirocitos. No tienen ninguna conexión luminar con el exterior de la glándula y constituyen, tanto estructural como funcionalmente, la unidad primaria secretora de este órgano. Las cc del folículo son las productoras de las hormonas tiroideas que las segregan a la luz del folículo que las almacena.
Su número puede ser de hasta tres millones. En la glándula adulta su tamaño es muy variable, siendo el diámetro desde 50 µm hasta 1mm de diámetro y como medida promedio 300 µm. El epitelio cuboidal que forma las paredes del folículo suele tener 15 µm. El interior del saco o folículo está lleno de un coloide homogéneo compuesto por un mezcla de proteínas, fundamentalmente tiroglobulina, si bien hay además iodoproteínas, proteínas del suero y albúmina.
En los estados de deficiencia de TSH este epitelio aumenta en altura, tomando forma columnar a la vez que aumenta la reabsorción del coloide reduciéndose el tamaño de la luz folicular a favor del epitelio, siendo la altura del epitelio inversamente proporcional al diámetro del folículo.
La cápsula tiroidea emite hacia el interior de la glándula unos septos de tejido conectivo que la dividen en lóbulos compuestos de unos 20-40 folículos. Los folículos están separados entre sí por tejido conectivo interfolicular que posee una rica red capilar que rodea el folículo.
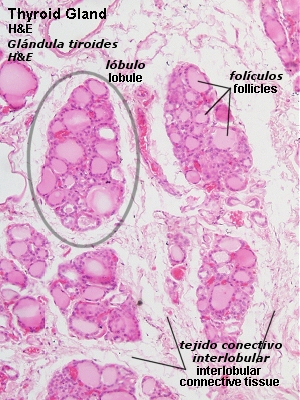 Además de las cc foliculares en el Ti hay otro tipo de cc llamadas cc C o parafoliculares que son las productoras de calcitonina, encontrándose situadas en los espacios interfoliculares o intersticio tiroideo, formando pequeños grupos arracimados, suponen el 1% de la población celular tiroidea.
Además de las cc foliculares en el Ti hay otro tipo de cc llamadas cc C o parafoliculares que son las productoras de calcitonina, encontrándose situadas en los espacios interfoliculares o intersticio tiroideo, formando pequeños grupos arracimados, suponen el 1% de la población celular tiroidea. Histológicamente, estas cc son difíciles de identificar. Recordar que la calcitonina, o tirocalcitonina, es la hormona que regula la concentración de calcio en el suero y mediante el sistema ladenilato-ciclasa-ciclic-adenosine monofosfato (cAMP), controla la reabsorción ósea. Las cc C contienen además somatostatina, calcitonia, gastrina, catacalcina y helodermina sustancias que tiene todas algún efecto estimulador o inhibidor del Ti. Estas cc tienen su origen embriológico en la cresta neural vía el último arco branquial y son el origen de los cánceres medulares del Ti.
Fuera de los folículos en la glándula hay además otros dos tipos de cc: cc endoteliales y fibroblastos.
Los tirocitos presentan una cara apical en contacto con el coloide, y otra cara basal orientada hacia el exterior del folículo.
La organización del folículo y la polaridad de los tirocitos son esenciales en el metabolismo tan especializado de este órgano: transporte de la tiroglobulina y del yoduro al ápice, síntesis de las hormonas tiroideas y su transporte a la membrana apical, almacenamiento del yodo y de la hormona tiroidea en forma de tiroglobulina en su luz y la endocitosis de la tiroglobulina también hasta el ápex celular. El comienzo de estas funciones celulares se inicia con la formación de esta estructura en el embrión.
Las cc acinares vistas con el microscopio aparecen lisas y aisladas, pero vistas con el M/E se muestran recubiertas por pequeñas vellosidades y se ve que poseen pseudópodos que las entrelaza.
En su base cada célula tiene un capilar.
Cada cc emite un cilio hacia la luz folicular.
Teñida con hematoxilina-eosina su citoplasma es neutrófilo, contiene vacuolas de coloide y su núcleo está en la base. El coloide suele tener una respuesta diferente a la tinción, así cuando la cc está en reposo es eosinofílico y cuando está en actividad o es estimulada se hace basófilo.
Las vellosidades que recubren estas cc son prolongaciones del citoplasma por lo que suponen un aumento de la superficie secretoria celular. Cuando el tiroides es muy estimulado los pseudópodos se extienden hacia fuera en el coloide, lo rodean y lo ingieren por macropinocitosis. Al cabo de unas horas, las gotas ingeridas se acercan a la base celular. Estas gotas de coloide reabsorbidas son transformadas en hormona por la glándula.
Al M/E puede observarse que los tirocitos están recubiertos por una membrana citoplásmica continua e ininterrumpida. Su parte apical posee numerosas microvellosidades de aproximadamente 0.35 mm alto y 0.07 mm ancho. Esta membrana está compuesta de dos capas oscuras separadas por una capa pálida y tiene 70 Å de espesor. Las cc están unidas unas a otras por los demosomas y en su parte apical por unas barras terminales. En las microvellosidades pueden observarse vesículas de uno 60 mm de ancho, conteniendo en su interior un material de la misma densidad que el coloide.
Por debajo del ápice hay una franja de citoplasma de unos 0´5 mm de ancho desprovista de todo tipo de órganos celulares, sólo se aprecian en este espacio microtúbulos y estructuras microfilamentosas. Bajo de esta franja aparecen las vesículas apicales que miden de 400 a 15.000 Å, y por debajo extendiéndose hasta la base celular está el retículo endoplásmico o ergoplasma, también conocido como vesículas ergoplásmicas.
Las vesículas ergoplásmicas, poseen una sola membrana, la citomembrana, de aproximadamente 60-70 Å de espesor, y su superficie exterior esta rodeada de ribosomas de un diámetro aproximado a 130-150 Å. En algunas áreas la citomembrana está desprovista de partículas del ribonucleoproteina, y entre las vesículas pueden verse gránulos de ribonucleoproteína libres. Estas vesículas son muy pleomórficas.
Cerca de la superficie apical pueden verse pequeñas vesículas de 50 nm a varias micras de diámetro que poseen una membrana de tan solo 5 nm de espesor. Estas vesículas a forma de gotas aparecen en el ápice de la cc para ser segregadas. Su contenido es generalmente es bastante denso. En los tiroides muy estimulados estas vesículas aparecen de un tamaño más grande, superiores a 1 micra. Se denominan gotas de coloide porque el contenido de estas vesículas es homogéneo y tiene la densidad del coloide y se forman por la endocitosis del coloide.
Estas cc poseen mitocrondrias de aspecto irregular. Su tamaño promedio es de 0.2 mm y poseen una triple membrana de 160 Å de grosor que consta de dos capas opacas y otra intermedia menos opaca. La capa interna forma unos pliegues hacia el interior de la mitocondria.
El núcleo posee una doble cubierta estando ambas capas separadas por un espacio denso de unos 200 Å de espesor. La membrana celular exterior es continuación del retículo endoplásmico. La envoltura del núcleo tiene unos poros característicos de 400 Å de diámetro.
La membrana plasmática en el área adyacente a la cc siguiente tiene unos 70 Å de grosor. Las cc están separadas entre si por un espacio vacío de unos 150 Å y que contiene un material similar a la membrana basal sobre la que se apoyan estas cc. La membrana basal esta formada por una fina capa de fibras y tiene una anchura de 400 Å. La membrana basal de la cc folicular está separa por un área clara de la membrana basal del endotelio de los capilares. La pared endotelial se interrumpe a intervalos frecuentes por un poro de 450 Å de diámetro. En estos puntos la luz capilar parece estar en contacto directo con la membrana basal de la cc endotelial. Las cc foliculares están separadas por dos capas de la membrana basal de los capilares, pero los poros del endotelio capilar pueden permitir que algo de plasma esté en contacto directo con la membrana basal. Esta estructura permite la libre difusión de materiales hacia dentro y fuera de la cc acinar.
Los ribosomas del ergoplasma sintetizan la tiroglobulina que se procesa en el retículo liso y en el aparato de Golgi.
El coloide de la luz folicular está cerrado herméticamente por la barrera celular y las uniones intercelulares:
- La uniones firmes de la zona oclusora que cierra los bordes apicales (occludins).
- Lejos del ápice están unas uniones muy firmes denominadas adherencias (cadherins).
- Los desmosomas.
Todas estos tipos de uniones intercelulares están unidas al citoesqueleto. Estas uniones permiten el paso de pequeñas moléculas de unas cc a otras.
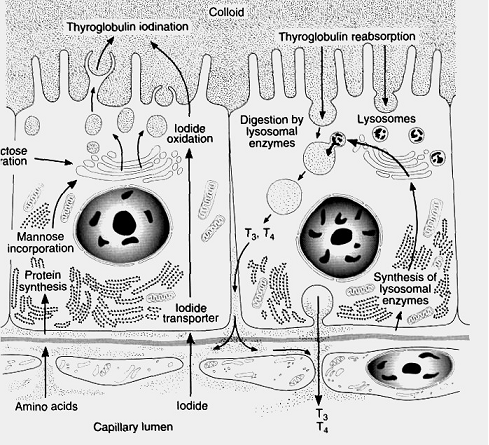
El metabolismo del Ti en relación con la síntesis de hormonas se expone en el capítulo siguiente. Aquí realizamos un revisión de algunos aspectos generales de metabolismo de la cc acinar tiroidea.
Energía metabólica.
La cc tiroidea precisa de energía para realizar sus actividades: síntesis de nucleótidos, proteínas, ácidos nucleares y lípidos, así como para sus funciones de transporte y otras actividades como la fagocitosis, movimientos lisosómico, etc. El 85% de la energía necesaria está producida por la fosforilación oxidativa de las mitocondrias y en menor cantidad por la glicolisis aerobia, o respiración celular.
Los valores absolutos de la captación de oxígeno, la captación de glucosa y formación del lactato son significativamente menores en las preparaciones humanas que las observadas en otros animales.
Para la obtención de energía en todas las cc del cuerpo humano es necesaria la participación del ribonucleótido adenosina trifosfato (ATP), dependiendo su intervención en gran parte de su concentración. En la cc tiroidea está en concentraciones milimolares y el 90% de los ribonucleótidos están en forma de trifosfatos que actúan como una gran fuente de energía para las cc.
La fuente principal de energía para las cc tiroideas son los ácidos grasos libres y su respiración se puede mantener “in vitro” por periodos muy largos en ausencia de aporte de un sustrato exógeno. En esta situación apenas hay glucógeno por lo que lo más posible es que sean los ácidos grasos libres su sustrato endógeno energético. Ahora bien, dada la compartimentación de estas cc puede ser que la glucolisis aeróbica generando moléculas de alta energía como la ATP sea la fuente de energía para algunas funciones membranosas como la endocitosis del coloide. De hecho la inhibición de la glucolisis inhibe la endocitosis del coloides mucho más que el el resto del metabolismo total de la cc y la adicción de glucosa neutraliza este fenómeno.
Con respeto a los efectos de la TSH sobre el metabolismo celular tiroideo se ha observado:
- Que los inhibidores mitocondriales pueden abolir el efecto estimulador de la TSH en la respiración de la cc tiroidea.
- Que el efecto estimulador de la TSH en la respiración celular es secundario al efecto que ejerce sobre el consumo de energía en los procesos celulares (por ejemplo sobre el ATP).
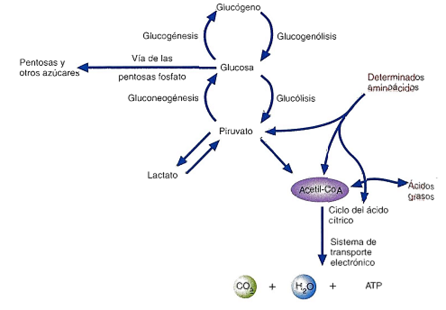 Metabolismo de los carbohidratos.
Metabolismo de los carbohidratos. Como ya hemos dicho, si bien la fuente principal de energía en los procesos metabólicos de la cc tiroidea son los ácidos grasos libres, el metabolismo de la glucosa tiene también su importancia en la función celular tiroidea como suministrador de energía.
Un 5% de la glucosa se catabolizada por la vía de Embden-Meyerhof (vía metabólica de la glucolisis anaeróbica) y mediante el ciclo de Krebs. Otro 6% de la glucosa se incorpora a las proteínas y menos del 1% a los lípidos y al glucógeno. El resto, que sería como un 10% se oxida por la vía de la hexosa monofosfatasa (HMP). La mayoría de los encimas que participan en la vía de Embden-Meyerhof, en el ciclo de Krebs y en HMP se han podido localizar en el tiroides humano.
El 70% de la glucosa suministradas a preparaciones tiroideas humanas y de perros se transforma en en el metabolito lactato, lo que significa que el metabolismo de la glucosa se ha realizado en condiciones de insuficiente oxigeno.
En el tiroides existe hexoquinasa en lugar de glucoquinasa; esta es una enzima citoplásmica que participa en la vía glucolítica llevando a cabo la fosforilación de glucosa a glucosa-6-fosfato. El grado de fosforilación de la glucosa (conversión de la glucosa en glucosa-6-fosfato que la prepara para nuevas reacciones metabólicas) probablemente es independiente de su concentración debido al bajo Km (parámetro que expresa la concentración de glucosa a la cual se tiene la mitad de la velocidad máxima de transporte) de hexoquinasa para la glucosa.
El metabolismo de la glucosa tiene varias fines:
- La incorporación de glucosa se relaciona con la síntesis de tiroglobulina por las cc tiroideas ya que esta hormona contiene un 10% de hidratos de carbono.
- El metabolismo de la glucosa por vía de la HMP se relaciona con la formación por esta vía de NADPH y pentosas. La NADPH es la nicotinamida adenina dinucleótido fosfato, que es una coenzima reducida que juega un papel clave en la síntesis de los hidratos de carbono en los organismos fotosintéticos. La producción de NADPH es necesaria para la generación del H2O2 por oxidación, para hacer que el I sea orgánico y para la síntesis de las hormonas tiroideas. El NADPH es también un cofactor muy importante para la desiodización de las iodotiroxinas, es también necesario para reducir la oxidación del glutation después de su generación por la glutatioperoxidasa en la detoxificación del H2O2 que pierde la cc. La formación de pentosas (monosacáridos) evidentemente es necesaria para la formación de nucleótidos.
La respiración mitocondrial.
La mitocondria ha sido denominada como el motor de la cc. Proporcionan el 85% del ATP que se forma en la cc tiroidea, mientras que solo el 15% se forma mediante la glucolisis. Se han estudiado las cc del Ti de múltiples especies y todas tiene mictocrondrias con la morfología y funciones típicas de las mismas: transporte de la cadena de electrones, encimas del ciclo de Krebs, fosforilación oxidativa y control respiratorio. La actividad de la mitocondria está controlada por los niveles de adenosina difosfato. La respiración también se vincula con la acumulación de Ca++ que juega un papel fundamental y general en la fisiología celular en los vertebrados.
Los ácidos graso libres son el mayor sustrato oxidativo en el Ti no estimulado, se supone que por la vía de las mitocondrias.
La respiración celular tiene su origen en gran parte en las mitocondrias y está estimulada en su actividad por la TSH con el consecuente consumo de ATP.
Está comprobado “in vitro” que la TSH aumenta el consumo del tiroides en un 20-30% durante algunos minutos, independientemente de los aportes exógenos.
La TSH estimula en el tiroides la oxidación del pirubato y del acetato. Compuesto como el perclorato, metamizol, ido, tiocianato y T4 no tiene una cción significativamente directa sobre la mitocondria. La síntesis de proteinas por parte de las mitocondrias exige un transporte de electrones y una fosforilación oxidativa perfectos e intactos. Esta última puede ser inhibida por el coramfenicol, pero sin embargo no por la cicloheximida que es un inhibidor de la síntesis de proteínas utilizado en cultivos.
Metabolismo del ARN y del ADN.
Cuando la TSH produce una estimulación crónica de la GT hay una hipertrofia de las cc tiroideas y un aumento de su proliferación debido a que se produce un aumento en la síntesis de ARN y ADN. La síntesis de ARN y de ADN son necesarias para el crecimiento y división celular. La TSH estimula además la captación e incorporación de los componentes-precursores para la síntesis de ARN y se ha comprobado como a las 12 horas de producirse la estimulación de la captación de precursores por parte de la TSH hay ya un aumento neto del ARN. Está comprobado como la TSH estimula la captación de precursores para la síntesis de purina y pirimidina.
Igualmente la TSH estimula la síntesis del ARN mensajero y del ARN ribosómico. El ARN mensajero es sintetizado preferente por estimulo de la TSH, tomando parte muy importante en su síntesis el AMP cíclico, y supone una expresión genética específica de la GT. No se sabe si la degradación del ARN está influenciada por la TSH.
Las poliaminas son moléculas alifáticas nitrogenadas cuyas principales funciones son: el empaquetamiento de ácidos nucleicos, la modulación de receptores de membrana y canales iónicos, la regulación de la expresión génica, inducción de la apoptosis y participación en el ciclo celular. La formación de poliaminas guarda una estrecha relación con el crecimiento celular pero se desconoce porque mecanismo. La TSH y el AMP cíclico mejoran la actividad del encima ornitina decarboxilada, cuyo nivel limita la síntesis de poliaminas.
Metabolismo celular de las proteínas.
El tejido de la GT está compuesto por cc y un almacén de proteínas y el funcionamiento de cada unos de sus compartimentos varia enormemente según la situación en que se encuentre la glándula. Así por ejemplo el almacenamiento y degradación de las proteínas del coloide se realiza al mismo tiempo y su contenido refleja en cada momento el balance entre estas dos actividades.
Está demostrado que la TSH mejora la captación de aminoácidos por parte de las cc tiroideas y estimula la síntesis de proteínas.
Metabolismo celular de los lípidos.
Los ácidos grasos libres son el combustible principal de la cc tiroidea y su oxidación es una gran fuente de energía metabólica. Existe suficiente sustrato endógeno para mantener la respiración durante varias horas durante la incubación in vitro de cortes de tejido tiroideo. Estudios sobre la localización de lípidos en los tiroides humanos normales haqn detectado cantidades apreciables de fosfolípidos, colesterol y gangliósidos: 5,2, 4,3 y 0,12 mmol/kg en tejido fresco. Las células C contienen la mayoría de los fosfolípidos. En paciente con bocios tirotóxicos sólo se pueden observar pequeñas cantidades de ellos. El tiroides humano contiene fosfolípidos en estas proporciones: fosfatidilcolina (41,8%), fosfatildiletanolamina (26,9%), fosfatidilserina (10,4%), fosfatidilinositol (4,4%), cardiolipina (3,4%), esfingomielina (12,4%). La TSH aumenta la incorporación de precursores para la mayoría de los fosfolípidos mediante una estimulación directa de la síntesis de fosfolípidos. Sin embargo, como la TSH también estimula la degradación de los fosfolípidos, el aumento de la síntesis de los fosfolípidos bajo la influencia de la TSH podría corresponder en parte a una aceleración de la renovación y no a una acumulación. La TSH también estimula la incorporación de inositol (vitamina B) a los los fosfoinosítidos (fosfolípidos celulares mensajeros) en un sistema libre de glucosa.
La TSH mejora específicamente la síntesis de ácido fosfatídico (lípido compuesto por glicerol) a partir de glicerofosfato (metabolito intermedio en el metabolismo graso) tras su administración in vivo.
Transporte y metabolismo electrolítico.
El potencial transmembrana en reposo estudiado en las cc tiroideas de ratas, conejos y cobayas varía entre -60 y -70 mV. La magnitud de este potencial depende principalmente del gradiente de K+ a cada lado de la membrana. Mantiene una concentración alta intracelular de K+ y baja de Na+, este gradiente se mantiene mediante la enzima Na+ - K+ ATPasa. Esta encima es sensible a la ouabaina que es un glucósido cardiaco de acción rápida que inhibe la bomba Na-K.
La actividad de esta ATPasa varía en relación directa con la estimulación crónica de la TSH, produciendo hipertrofia celular e hiperplasia. No hay evidencia de como se realiza la acción directa de la TSH sobre esta enzima. La estimulación aguda de las cc tiroideas induce una despolarización de la cc, que se acompaña de una disminución de la resistencia de la membrana.
La despolarización de la cc puede corresponder también a un aumento de la permeabilidad a cationes predominantemente extracelulares, como Na+, o a una disminución de la permeabilidad a cationes predominantemente intracelulares, como K+. La administración de TSH o veratridina, alcaloide agonista del canal de Na+, despolariza las cc tiroideas cultivadas y aumenta la secreción de yodo radiactivo unido orgánicamente. Por el contrario la despolarización de las cc mediante el aumento de la concentración de K+ en el medio no logró promover la secreción de yodo radiactivo, lo que indica que la afluencia de Na+, y no la despolarización en sí misma, puede mediar en la respuesta secretora.