-
Medidas generales.
-
Tratamiento postural.Dilatadores nasales.
-
Tratamiento farmacológico.
-
Dispositivos intraorales.
-
Oxigenoterapia.
-
CPAP.
El SAOS ha de ser tratado siempre habiendo comprobado que los pacientes no tratados tienen una mortalidad significativamente más alta que los tratados. El tratamiento del SOAS es multifactorial abordando diversos aspectos no excluyentes entre sí. Consta de unas medidas generales aplicables todos los casos y de métodos instrumentales y quirúrgicos.
MEDIDAS GENERALES.
Son de aplicación en todos los casos.
- Obesidad: el adelgazamiento es la primera medida que se debe tomar en pacientes obesos con roncopatias, debiendo hacerlo enérgicamente, si bien pocas veces se consiguen logros significativos a largo plazo. La simple reducción de un 5-10% del peso corporal se suele acompañar de una disminución en el número de apneas y una mejoría de la hipoxia crónica, reduciendo la gravedad del cuadro y mejorando su mortalidad. Incluso las técnicas quirúrgicas del SAOS tienen un mejor pronóstico en los sujetos que logran perder peso. Al adelgazar disminuye el grosor del tejido adiposo del cuello mejorando el calibre de la VAS con el consiguiente alivio mecánico. También se ha sugerido que una dieta hipocalórica, pobre en hidratos de carbono, origina un estado de cetosis suficiente como para estimular el centro respiratorio. La reducción del sobrepeso se considera tan importante que incluso en determinados casos puede estar indicado el tratamiento quirúrgico del mismo mediante técnicas de cirugía bariátrica. Cuando la obesidad es mórbida se requiere tratamiento de la enfermedad causal.
- Higiene de sueño: intentar que el paciente lleve una regularidad en los hábitos de sueño.
- Se recomienda no tomar alcohol en las cenas e incluso durante el día, pues aumenta la somnolencia diurna.
- Supresión de todo tipo de fármacos que pueden agravar el cuadro, como son los hipnóticos o depresores del SNC, particularmente por la tarde noche. Igualmente se aconsejará no tomar miorrelajantes, diazepán o reserpina. Es frecuente que pacientes con SOAS tomen este tipo de fármacos que han sido prescritos al referir insomnio o sueño agitado. Igualmente se han de prohibir los betabloqueantes y los andrógenos.
- Se ha de evitar el tabaco y otros hábitos nocivos. El abandono del hábito tabáquico plantea muchas veces un problema de sobrepeso secundario.
- El paciente debe de ser informado además de las repercusiones del SAOS para su estado general de los riesgos que supone la somnolencia para sufrir accidentes industriales o de automóvil.
 TRATAMIENTO POSTURAL.
TRATAMIENTO POSTURAL.
Se ha de pretender que el paciente mantenga durante el sueño una postura que evite una propulsión hacia atrás de las partes blandas de la VAS, teniendo este tratamiento especial interés en aquellos paciente en los que el cuadro sólo se produce cuando duermen en decúbito supino. Con el decúbito supino, por acción de la gravedad, esta zona blanda es propulsada hacia atrás, y en decúbito prono, cae hacia adelante, por lo que la posición ideal a adoptar será esta última. La importancia de la postura al dormir es evidente al punto que algunos pacientes con roncopatía crónica sólo presentan los ronquidos y apneas en decúbito supino. Si estos pacientes logran descansar boca abajo no sólo dejarán de roncar sino que mejorarán el cuadro clínico.
Cuando se trata de pacientes obesos, al dormir boca abajo con un abdomen voluminoso, hace que la compresión de éste dificulte la respiración. Los obesos son pacientes que se someten mal al tratamiento postural, tanto por imposibilidad física como por falta de motivación.
La mejor postura seria dormir boca abajo con la frente apoyada sobre el antebrazo, de tal manera que la mandíbula inferior, lengua y velo del paladar caigan hacia delante, con lo que la vía aérea superior queda libre y no se producirán ronquidos ni apneas, a condición de que las fosas nasales estén permeables. Esta posición es útil y soportable por algún tiempo, pero no es posible mantenerla durante toda la noche, entre otros motivos por las molestias que se producen en el brazo y la espalda. Cuando existe una obstrucción nasal ésta sigue siendo la mejor posición, pero es peor soportada que en condiciones de buena permeabilidad nasal.
Más útil que la postura anterior suele ser el decúbito lateral, ya que si bien es menos efectivo que el prono es mejor soportado. Para que el paciente corrija durante el sueño la posición de decúbito supino se han ideado multitud de dispositivos, solo en EE.UU. existen más de 300 aparatos patentados, siendo el más conocido la pelota de tenis en la espalda y los aparatos electrónicos basados en los reflejos condicionados de Pavlov que obligan a cambiar de postura cuando el ronquido sube de intensidad sonora. El tratamiento postural puede ser muy útil en roncopatías simples, en el SAOS suele ser tan solo una medida coadyuvante a la mejoría.
Se ha propuesto también la utilización de un collar cervical, similar al utilizado en los esguinces de cuello, para utilizarlo durante la noche manteniendo elevado el mentón con lo que se pretende prevenir la protrusión lingual y la flexión de la tráquea. Puede ser útil, si se tolera, en algunas personas con ronquido en decúbito supino.
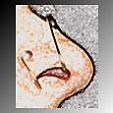 DILATADORES NASALES.
DILATADORES NASALES.
Consisten en unas prótesis de silicona que abren las narinas mejorando la respiración nasal al suprimir la resistencia de la válvula nasal, por lo en particular son muy efectivos cuando hay colapso alar. La misma función tienen las tiritas adhesivas externas.
TRATAMIENTO FARMACOLOGICO.
Ningún fármaco ha demostrado ser totalmente eficaz en el tratamiento de la roncopatía ni en el SAOS. Se han utilizado varios fármacos para intentar estabilizar la vía aérea superior, incrementar el impulso ventilatorio y mejorar la actividad de la musculatura respiratoria, consiguiendo algunos de ellos tan sólo algunos resultados muy discretos.
- Proptriptilina: antidepresivo tricíclico no sedativo. En algunos casos de roncopatías y SOAS leves puede proporcionar algún beneficio por su efecto estimulante de los músculos de las VAS y particularmente durante las apneas del sueño REM. Se ha observado que las fracciones de sueño con caídas de la oxihemoglobina son menores, disminuyen las apneas y los despertares nocturnos. Se comienza por dosis de 5 mg, aumentando progresivamente hasta la dosis eficaz sin sobrepasar los 30 mg. y vigilando posibles efectos secundarios. Se indican para casos de SAOS leves o en aquellos enfermos que rechazan otros tipos de tratamientos más agresivos. También se ha utilizado la clomipramina.
- Azetazolamida: inhibidor de la anhidrasa carbónica que actúa provocando una acidosis metabólica a nivel del túbulo renal, estimulando así la respiración. Además puede aumentar la presión de dióxido de carbono a nivel cerebral por bloqueo del transporte del dióxido de carbono, pudiendo cesar la formación de bicarbonato a nivel del LCR, provocando como consecuencia un aumento sostenido de la ventilación alveolar. Está demostrada su eficacia en las apneas centrales y puede mejorar parcialmente las apneas obstructivas por su efecto estimulante respiratorio. Las apneas centrales se desencadenan en medio alcalino, por lo que este fármaco actúa alterando esta situación metabólica. Se administra en dosis única nocturna de 250 mg vigilando sus contraindicaciones. Su utilización es controvertida, así hay estudios que demuestran tan sólo una mejora de las peculiaridades psicológicas del cuadro sin afectar al resto de la sintomatología, y en contraposición otros estudios muestran su utilidad en las apneas centrales y en las que se producen en el síndrome de Arnol-Chiari.
- Progesterona y derivados: en el hombre y en la mujer postmenopáusica estos trastornos son estadísticamente más frecuentes por lo que se han relacionado con la disminución de hormonas sexuales. La progesterona aumenta la ventilación alveolar durante el embarazo y la fase luética del ciclo menstrual. El acetato de clormanidona diminuye los episodios de apnea e hipoxia mejorando el patrón de sueño, sin embargo no altera la relación despertares nocturnos – índice de apneas-hipopnea. En obesos hipercápnicos con SAOS se ha indicado acetato de medroxiprogesterona, 60 mg/día, siendo controvertida su eficacia. Algunos autores han indicado la administración conjunta de medroxiprogesterona y antidepresivos tricíclicos.
- Nicotina: es un estimulante respiratorio que no se utiliza por sus numerosos efectos secundarios, si bien su administración en pacientes con SAOS ha demostrado que produce una disminución en el número y duración de apneas con un efecto transitorio ya sólo actúa en las dos primeras horas del sueño. Igualmente se ha objetivado que aumenta la ventilación-minuto.
- Almitrina: es un estimulante central de la respiración sin apenas efectos secundarios. Aumenta la ventilación, habiéndose comprobado que aumenta la presión arterial de O2 sin modificar la presión arterial de CO2, de la misma forma que se ha observado un incremento en la relación ventilación-perfusión. Sus resultados en SAOS no pueden calificarse de positivos.
- La estricnina: actúa como bloqueante por inhibición postsináptica.
- En paciente con bloqueo nasal por rinitis pueden utilizarse descongestivos nasales y esteroides inhalados.
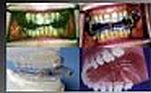 DISPOSITIVOS INTRAORALES: PEB.
DISPOSITIVOS INTRAORALES: PEB.
Constituyen otra alternativa terapéutica, incruenta, reversible, sencilla de realizar, que no conlleva complicaciones ni secuelas y cuyo coste es bajo. Se trata de una serie de dispositivos estomatológicos o prótesis endobucales diseñadas para aumentar las dimensiones anteroposteriores de la faringe. Se indican en casos de no tolerancia del CPAP y cuando se rechaza, fracasa o está contraindicada la cirugía. Existen fundamentalmente tres tipos de ortesis:
· Retenedor de la lengua (Tongue-Retaining Device o TRD): se adapta a la anatomía del paciente ajustándose al maxilar y manteniendo la lengua adelantada. Su tolerancia no sobrepasa el 50% de los casos y precisa de una vía nasal permeable. En la práctica no es un dispositivo muy eficaz, por lo que prácticamente no se utilizan.
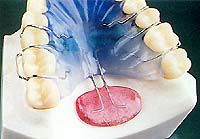 · Prótesis para elevación del velo palatino. Pacientes con exceso de tejido blando en la región orofaríngea obstruyendo la vía aérea. Uno de estos aparatos tiene un botón de acrílico que se extiende distalmente hasta un punto en el medio del paladar que levanta el tejido previniendo la vibración durante la circulación del aire. Su eficacia no es ampliamente aceptada por los pacientes ya que induce el reflejo del vómito. Ha sido aprobado solo para roncadores y no para SAOS.
· Prótesis para elevación del velo palatino. Pacientes con exceso de tejido blando en la región orofaríngea obstruyendo la vía aérea. Uno de estos aparatos tiene un botón de acrílico que se extiende distalmente hasta un punto en el medio del paladar que levanta el tejido previniendo la vibración durante la circulación del aire. Su eficacia no es ampliamente aceptada por los pacientes ya que induce el reflejo del vómito. Ha sido aprobado solo para roncadores y no para SAOS.
· Prótesis de avance mandibular: PMA. Estas prótesis propulsoras de la mandíbula fueron propuestas en 1934 como tratamiento de las VAS durante el sueño por Pierre Robin en 1934. este autor utilizaba una ortesis monobloque con el fin de propulsar hacia delante la mandíbula para ensanchar las VAS en los niños con micrognatia. Posteriormente Cartwright ampliaba esta indicación al tratamiento intraoral del SAOS. Son las más utilizadas. Son prótesis de ortodoncia construidas según las medidas celafalométricas del paciente que se utilizan solo por la noche y avanzan la mandíbula cambiando así la posición de la lengua, además mantienen la boca abierta. Todas ellas poseen un anclaje dental constituido por un entablillado de resina sintética, elaborado a partir de un molde de yeso de la arcada dental.
La eficacia de las PMA es evidente haciendo disminuir los valores promedios del índice de apneas-hipopneas, si bien su mecanismo de acción no se conoce con exactitud. El avance mandibular modifica poco o nada el espacio retrolingual; el descenso mandibular conlleva el de la base de la lengua que toma una posición más inferior sin acercarse a la pared posterior de la faringe; la apertura bucal y el descenso de la lengua se traducen en un agrandamiento de la cavidad bucal; la nueva posición de la mandíbula y de la lengua entraña un cambio de posición del velo del paladar, que se desplaza hacia delante, y debido a ello, aumenta el espacio retrovelar reduciendo la posible obstrucción velofaríngea; en todos lo estudios efectuados se ha constatado que se produce una disminución de la distancia que separa el hueso hioides del plano mandibular. Estos cambios de posición de la mandíbula, la lengua, el velo del paladar y el hueso hioides modifican las propiedades de la faringe disminuyendo su capacidad para colapsarse al aumentar la tensión y la rigidez del velo palatino y de las paredes faríngeas. Además se ha demostrado que el tono de los músculos genioglosos, que disminuye de manera significativa durante las apneas obstructivas, aumenta con los movimientos de apertura de la boca.
En general son bien toleradas, pero pueden presentar intolerancias que varios motivos: no obtener una mejoría clínica, inestabilidad de la prótesis, dolores dentales o en articulaciones TNM, modificación de la oclusión dental, incontinencia salival y sequedad bucal.
Son contraindicaciones: la no existencia de dientes sólidos para la aplicación de la prótesis, las disfunciones de la articulación TNM.
La prótesis necesita de una revisiones por desgaste.
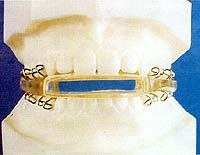 Existen tres tipos de aparatos PMA:
Existen tres tipos de aparatos PMA:
- Aparatos monobloc: están hechos de una sola pieza por la unión de las tablillas maxilares y mandibulares. Estos aparatos son a menudo voluminosos e incómodos de colocar en la boca. La posición de la mandíbula queda bloqueada, con una cuantía de abertura bucal y de propulsión predeterminada y no ajustable, salvo remodelación de la prótesis. La ausencia total de movilidad mandibular puede hacerla incómoda y entorpecer la deglución nocturna de saliva. En caso de que se desencaje de la mandíbula, puede ser difícil colocarla en su lugar.
- Tablillas independientes: se colocan por separado entre sí y se solidarizan mediante un sistema de fijación que determina la cuantía de propulsión y de apertura bucal. Aunque son más prácticas para colocarlas en la boca, adolecen de los mismos inconvenientes que las monobloc por lo que respecta a la pérdida de los movimientos mandibulares.
- Activadores mandibulares: utilizan las bielas de Herbst para articular las dos tablillas. Su acción propulsora no se efectúa más que con los movimientos de cierre de la boca (deglución). Para obtener una propulsión mandibular nocturna en el tratamiento del SAOS, es absolutamente necesario, por tanto, lograr un cierre bucal pasivo mediante la adición de un dispositivo de bloqueo intermaxilar con elementos elásticos, aunque existe el riesgo de desinserción de la prótesis a causa de los mismos. La amplitud de la propulsión puede regularse fácilmente por medio de las bielas.
OXIGENOTERAPIA.
Basándose en que la hipoxemia es en parte causante de la sintomatología del SAOS, comenzó a utilizarse para su tratamiento. Se demostró que no es un tratamiento eficaz para el mismo, ya que no tiene ningún efecto sobre la hipersomnia y provoca, en ocasiones, una hipercapnia significativa.
Unicamente se encuentra indicada en el síndrome overlap. En algunos laboratorios de polisomnografía y para algunos casos, se incluye una prueba de utilización de oxigenoterapia para valorar su efecto durante el sueño.
 PRESION POSITIVA CONTINUA EN LA VIA AEREA: CPAP.
PRESION POSITIVA CONTINUA EN LA VIA AEREA: CPAP.
Consisten en la aplicación durante la noche de aire a presión positiva continua a la vía aérea superior a través de la nariz. Este tratamiento se comenzó a utilizar a partir de 1981 por Sullivan, si bien su uso no se popularizó hasta la aparición de modelos comerciales en la década pasada.
El aparato consta de un compresor que proporciona a la VAS aire a una presión predeterminada durante las dos fases del ciclo respiratorio mediante una mascarilla que ajusta herméticamente sobre la nariz del paciente.
El efecto del CPAP nasal es neumático-dilatador, creando una presión positiva en la vía aérea superior que contrarresta la presión negativa generadora de la oclusión faríngea al comienzo de la inspiración, es decir, que actúa como una férula neumática que impide el colapso faríngeo durante el sueño. El paladar blando durante su aplicación realiza un efecto de sellado o cierre de la cavidad faríngea que impide la fuga de aire hacia la boca. La presión necesaria para vencer la oclusión y evitar las apneas e hipopneas oscila entre 5 y 15 cm de agua, por lo que el riesgo de barotrauma o hipotensión por descenso del retorno venoso es despreciable. Para conseguir que la presión se mantenga constante a lo largo del ciclo respiratorio, los compresores reducen el flujo de aire suministrado durante la espiración al detectar que la presión aumenta debido al espirar el paciente y lo incrementan durante inspiración cuando esta disminuye, siendo las variaciones muy pequeñas como de 2 cm de agua. Posee además un dispositivo o válvula en la mascarilla nasal que evita la reinhalación del aire espirado, o bien simplemente de unos orificios de fuga.
El aparato se instala en la casa del paciente y consta de un generador de flujo que transmite el aire a través de un tubo a la mascarilla nasal que ha de colocarse el paciente.
El tratamiento exige de un control-seguimiento de su eficacia y tolerancia, siendo necesario ajustar bien la presión necesaria. Para conocer cual es la presión necesaria que ha de generar el aparato en cada paciente, se ha de ir ajustando ésta progresivamente durante un registro polisomnográfico nocturno hasta conseguir una presión que logre en todos lo estadios del sueño impedir las apneas y los ronquidos. A esto se denomina conseguir una CPAP óptima, que es la que se ha de mantener constante durante la respiración nocturna. Como esto es muy costoso, frente a este procedimiento, se ha diseñado otras estrategias, como es realizar sólo estudios de media noche, cálculos mediante registros cardiorespiratorios, fórmulas de predicción a partir del índice de masa corporal, IAH, y circunferencia del cuello. También se puede hacer una graduación automática en hospital o domicilio con un CPAP inteligente o auto-CPAP, que puede detectar la obstrucción de las VAS y generar la presión exacta para prevenir las apneas. Además se ha de hacer un control del cumplimiento y eficacia a largo plazo.
 Con el tiempo, los equipos que en un principio eran bastante engorrosos se han ido mejorando, consiguiendo compresores más silenciosos y menos pesados, mascarillas con mejor adaptación o su sustitución por olivas nasales en los casos de claustrofobia a las mismas. La modificación más importante ha sido los sistemas ventiladores de doble presión (BiPAP) que permite suministrar una presión diferente durante la inspiración y la espiración, lo que hace que el tratamiento se mejore mucho sobre todo en los pacientes que necesitan presiones de CPAP altas. Otro de los sistemas introducidos ha sido el sistema llamado de rampa, que consiste en la elevación progresiva de la presión administrada hasta llegar a la precisada por el paciente. Otra de las alternativas presentadas es la adición de oxigeno (especialmente indicada en el síndrome overlap) y sistemas de humidificación, lo que tiene un especial interés en paciente con EPOC. La última novedad al respecto es la aplicación de un microprocesador incorporado a la mascarilla que analiza las necesidades de presión del paciente, ajustando las cifras de presión a lo largo de la noche.
Con el tiempo, los equipos que en un principio eran bastante engorrosos se han ido mejorando, consiguiendo compresores más silenciosos y menos pesados, mascarillas con mejor adaptación o su sustitución por olivas nasales en los casos de claustrofobia a las mismas. La modificación más importante ha sido los sistemas ventiladores de doble presión (BiPAP) que permite suministrar una presión diferente durante la inspiración y la espiración, lo que hace que el tratamiento se mejore mucho sobre todo en los pacientes que necesitan presiones de CPAP altas. Otro de los sistemas introducidos ha sido el sistema llamado de rampa, que consiste en la elevación progresiva de la presión administrada hasta llegar a la precisada por el paciente. Otra de las alternativas presentadas es la adición de oxigeno (especialmente indicada en el síndrome overlap) y sistemas de humidificación, lo que tiene un especial interés en paciente con EPOC. La última novedad al respecto es la aplicación de un microprocesador incorporado a la mascarilla que analiza las necesidades de presión del paciente, ajustando las cifras de presión a lo largo de la noche.
Cuando el tratamiento de CPAP es tolerado se obtiene de forma inmediata un efecto beneficioso que va corrigiendo las alteraciones fisiopatológicas del SAOS. Así se observa una mejoría de la somnolencia diurna, las cefaleas, la astenia y los trastornos del carácter. Esta mejoría es progresiva durante el primer año de su utilización. Se corrige la hipoxemia y en consecuencia toda la sintomatología cardiovascular. Una utilización de al menos cuatro horas por noche es ya suficiente para reducir la somnolencia. Un solo día sin su uso provoca la recurrencia de la hipersomnia diurna. Cuando el paciente no refiere una mejoría subjetiva se ha de cuestionar el diagnóstico. Una reaparición de los síntomas durante el uso habitual de CPAP sugiere un aumento ponderal, o la ingesta de alcohol o de drogas miorrelajantes.
Antes de colocar un CEPAP se ha de valorar la función nasal, pues su obstrucción puede ser la causa una intolerancia a la máquina.
 Para muchos autores es el tratamiento de elección ya que corrige las apneas e hipopneas a pesar de desconocerse la(s) ziona(s) de obstrucción. Sin embargo, el cumplimiento de este tratamiento por parte de los pacienes puede ser bajo. Las indicaciones, como ocurre con el tratamiento quirúrgico, han de individualizarse a cada caso, en general está indicado en la mayoría de casos de SAOS grave y moderado. Para valorar la gravedad del cuadro se utilizan estos criterios:
Para muchos autores es el tratamiento de elección ya que corrige las apneas e hipopneas a pesar de desconocerse la(s) ziona(s) de obstrucción. Sin embargo, el cumplimiento de este tratamiento por parte de los pacienes puede ser bajo. Las indicaciones, como ocurre con el tratamiento quirúrgico, han de individualizarse a cada caso, en general está indicado en la mayoría de casos de SAOS grave y moderado. Para valorar la gravedad del cuadro se utilizan estos criterios:
- Asociación de síntomas cardiovasculares y de otras enfermedades respiratorias como el EPOC.
- Grado y frecuencia de las desaturaciones arteriales. Si bien nadie se atreve a dar unas cifras concretas.
- Número de apneas o hipoapneas, pudiendo considerarse como límite un índice de 20 apneas/hora o mayo. Para algunos autores con valorar este índice les basta para plantear la indicación. Para otros se han de asociar síntomas importantes como somnolencia en situaciones activas claramente valorable y limitante de las actividades, o episodios repetitivos de asfixia nocturna, o bien cuando se asocia patología cardiovascular o cerebrovascular relevante o enfermedades que cursan con insuficiencia respiratoria. Algunos autores suben este índice para considerarlo indicación a 30.
- Indice IAH > 30, sin sintomatología ni factores de riesgo. Esta indicación es controvertida y así para muchos autores estos pacientes no se consideran subsidiarios de CPAP nasal.
- Pacientes con síntomas claros de apneas o hipoapneas asociadas a factores de riesgo cardiovasular relevantes, aunque el índice de IAH sea inferior a 20 m.
- Cuando falla el tratamiento quirúrgico.
La tolerancia a corto plazo es buena, superior al 85% (15% de intolerancia inmediata), si bien en algunos casos no se tolera por la sensación de claustrofobia que puede producir la mascarilla, irritación cutánea local, el ruido del aparato, sequedad nasal, conjuntivitis, barotrauma ótico, etc. A largo plazo la tolerancia y el uso continuado disminuye al 70-65% de los casos prescritos, si bien en principio el tratamiento es para años, o de por vida.
Son contraindicaciones a la utilización de CPAP:
- Existencia de neumotórax o enfisema bulloso. Sólo se utiliza en SAOS muy graves.
- Infección de vías respiratorias superiores.
- Hipovolemia e insuficiencia cardíaca. El CPAP puede disminuir el gasto cardiaco cuando la presión es superior a 10 cm de H2O, por lo cual en estos casos la presión ha de ser inferior.
- Epiglotis laxa. La presión positiva puede desplazar la epiglotis y producir una obstrucción glótica, con el peligro consiguiente.
- Obstrucción nasal muy intensa: puede constituir una contraindicación, por la imposibilidad de soportar el sistema.
TRATAMIENTO QUIRURGICO DE LA RONCOPATIA.
Capítulos siguientes.
