-
Anamnesis.
-
Examen ORL.
-
Laboratorio.
-
Estudio básico funcional respiratorio.
-
Radiología.
-
Videofibrosomnoscopía.
-
Reflexión acústica.
-
Medición de presiones intrafaríngeas.
-
Evaluación cardiológica.
Los cuadros de SOAS suelen comenzar por una roncopatía como primera manifestación del estrechamiento de la faringe que es debida a la vibración de las partes blandas de la vía aérea superior, siendo el ruido inspiratorio el síntoma más común referido por el paciente o su pareja. El sonido va siendo cada vez más sonoro, como consecuencia del aumento de actividad de los músculos respiratorios que intentan vencer la limitación del flujo aéreo. En un determinado momento se produce el colapso de la faringe, lo que determina el comienzo de un período de apnea. Los movimientos tóraco-abdominales, estimulados por la hipoxemía y la hipercapnia, aumentan de forma progresiva, incluso se hacen paradójicos. Finalmente el silencio de la apnea se rompe con un ronquido estertoroso, que refleja el restablecimiento de la permeabilidad de la vía aérea. Los gases sanguíneos que durante la apnea se han alterado, se normalizan, el sueño se recupera y se reinicia así un nuevo ciclo que se repite múltiples veces cada noche.
El diagnóstico va a fundamentarse en la historia clínica junto a una serie de exploraciones complementarias que permiten saber si el pacinete es un roncador simple o presenta una forma más evolucionada. El diagnóstico ha de ser sindrómico y etiológico de tal forma que además de dar a conocer la importancia y transcendencia del cuadro, aporte información sobre la etiología del cuadro lo que permitirá determinar qué tratamientos serán los más eficaces para corregirlo.
 ANAMNESIS.
ANAMNESIS.
En general suele tratarse de un cuadro clínico muy llamativo y el interrogatorio ha de dirigirse además de al paciente, a las personas que conviven con él, ya que en la mayoría de los casos el propio paciente no acude voluntariamente a consultar, pues no valora, o minusvalora, sus manifestaciones clínicas.
La historia clínica ha de ser precisa y sistemática, haciendo un recorrido por la posible sintomatología, para lo cual se puede hacer una diferenciación en síntomas nocturnos y síntomas diurnos:
· Síntomas nocturnos.
- Ronquido intenso. Es el síntoma inicial, tiene una sensibilidad del 65%, con una especificidad cercana al 100%. En general molesta más a las personas que conviven con el roncador que a el mismo, ya que a pesar de que puede alcanzar intensidades de ruido por encima de los 85 dB, el roncador puede no ser consciente del mismo, lo que hace que sea un problema menos médico y más social y familiar. El nivel de ronquido más grande que se ha medido, ha sido de 87,5 dB en un roncador crónico del condado de Kent en Inglaterra. Suele ser mayor en decúbito supino y tras la ingesta de alcohol. En el SAOS suele tener una intensidad progresivamente creciente según avanza el sueño. Mediante la anamnesis y la simple observación clínica del sueño, en muchos casos, no se puede diferenciar una roncopatía simple de un SAOS y mucho menos se puede determinar la gravedad del cuadro.
- Respiraciones periódicas con pausas de apnea. Es el síntoma fundamental de SAOS. La persona que comparte habitación con el paciente dá evidencia de las pausas respiratorias nocturnas, de su duración aproximada y de su frecuencia.
- Actividad motora anormal. Los intentos para tratar de superar las crisis de apnea dan como resultado un sueño inquieto y agitado con mucho movimiento, sudoración nocturna y numerosos cambios de posición durante la noche. Pueden producirse sacudidas de los miembros superiores e inferiores, e incluso caídas de la cama. Los pacientes pueden sufrir pesadillas y somniloquia o sonambulismo. Pueden referir que se despiertan por la noche bruscamente con dificultad respiratoria: despertares nocturnos.
- Enuresis. Es rara en el adulto. Poliuria. Nicturia: es muy frecuente e intensa y tiene su explicación en una menor secreción nocturna de hormona antidiurética y en una mayor liberación del factor natriurético atrial.
- Insomnio, sobre todo al comienzo de la noche.
- Para vencer la obstrucción de la VAS se generan presiones intratorácicas y abdominales que suponen igualmente cambios significativos en las presiones esofágica y gástrica, lo que explica la posible aparición de sintomatología de reflujo gastroesofágico.
Toda ésta es la sintomatología nocturna es la que suele presentar el paciente con un síndrome de SOAS, perno no así el roncador simple que prácticamente sólo presenta ronquido en mayor o menor intensidad.
 · Síntomas diurnos.
· Síntomas diurnos.
- Hipersomnia diurna: es la tendencia a quedarse dormido de forma constante durante el día con el peligro que esto puede entrañar a lo largo de la actividad diaria. Es un síntoma que no falta en ningún caso, difícilmente vencible por parte del paciente, que unas veces sólo aparece tras la comida o al realizar actividades que no requieren actividad física (sentado), pero que en ocasiones aparece incluso realizando labores que precisan cierta actividad. A veces en el SAOS la somnolencia llega a ser tan severa que incapacita totalmente a estos enfermos en su vida diaria, pudiendo dormirse comiendo, conduciendo, e incluso hablando, etc. Esta hipersomnia se debe fundamentalmente a que estos pacientes no duermen bien durante la noche, ya que en las apneas sufren sobresaltos que los despiertan, o sufren despertares subconsciente con sensación de angustia y falta de respiración. La reiteración de estos fenómenos al final de cada apnea da lugar a la fragmentación del sueño, impidiendo un descanso profundo y reparador.
La somnolencia diurna se clasifica en:
- leve, cuando es poco frecuente, sólo en situaciones pasivas con poca repercusión en las actividades habituales;
- moderada, cuando son episodios que acontecen con cierta regularidad en situaciones que requieren cierto grado de atención;
- intensa, cuando son episodios de frecuencia diaria en situaciones activas que alteran de forma importante las actividades habituales.
Relacionados con esta situación pueden aparecer trastornos de la conducta (automatismo) y la personalidad (tendencia a la depresión, irritabilidad, paranoia, etc.), pérdida de memoria, deterioro intelectual, disminución de la habilidad motora y de la destreza perceptiva.
- Cefalea matutina: es bastante frecuente, se debe a la vasodilatación cerebral ocasionada por la hipercapnia que acompaña a las apneas. Aparece en la mitad de los casos.
- Alteraciones de la libido e impotencia sexual, que parecen tener su origen en una menor secreción nocturna de testosterona.
El interrogatorio incluye los antecedentes laborales, hábitos, medicaciones seguidas y patologías asociadas, especialmente las cardiorespiratorias y neurológicas. La anamnesis puede realizarse mediante un cuestionario dirigido que es más objetivo y ahorra tiempo.

EXAMEN ORL.
Si bien la mayoría de los autores están de acuerdo en la posible localización de la obstrucción a nivel del esfinter velofaringeo o en la base de la lengua, no existe unanimidad a la hora de enco0ntrar una exploración única que determine donde se encuentra la obstrucción, ni un método fiable con el que sentar una indicación de tratamiento.
La exploración tiene como finalidad la búsqueda de los factores etiológicos predisponentes, tanto estructurales (anomalías anatómicas) como funcionales de las VAS, ya que ambos tipos están estrechamente relacionados en la génesis de esta patología. El poder determinar en que puntos de las VAS se produce obstrucción encierra una gran dificultad. El uso y la utilidad de las diferentes pruebas que se exponen a continuación van a variar en cada caso, pues en ocasiones se utilizan para el diagnóstico etiológico y en otras para evaluar la evolución del paciente.
- Exploración general: atañe a la obesidad y situación cardiopulmonar. Tensión arterial.
- Exploración nasal: búsqueda de posibles causas obstructivas.
- Exploración rinofaringea igualmente en búsqueda de posibles causas obstructivas. La aparición del nasofibroscopio flexible ha facilitado enormemente esta exploración, permitiendo una visión endocavitaria directa de tipo morfológico y que además permite explorar la rinofaringe en diversas posiciones y circunstancias. Durante la rinofibroscopia en estos pacientes se ha de realizar la maniobra de Müller que permite una información funcional de la compliancia de las VAS: paciente en decúbito supino, tras introducir el fibroscopio se le indica que cierre la boca mientras se le tapan ambas narinas, en esta situación el enfermo debe de intentar realizar una inspiración forzada y observando el desplazamiento posterior de la base de la lengua, colapso de la hipofaringe y cierre a nivel del paladar blando. La maniobra valora el colapso hipofaringeo y el colapso velofaringeo. A esta maniobra se le ha dado una utilidad predectiva del éxito que vaya a alcanzarse con la cirugía, lo que es muy discutible. Sí que valora mejor los resultados postquirúrgicos.
Si la fibroendocopia se realiza durante el sueño es cuando aporta más información para el diagnóstico. Lo mismo ocurre con la videofibrosomnoscopia que luego se expone.
- Exploración bucal. Valoración del tamaño y posición lingual. Una retrognatia o micrognatia: están presentes en el 20% de estos pacientes. Ésta puede objetivarse y evaluarse mejor mediante la telerradiografia del cráneo con boca cerrada. Es importante valorar el tamaño de la arcada dentaria mandibular en relación con el tamaño de la lengua, ya que si el espacio del suelo de la boca es relativamente pequeño para una lengua de tamaño normal, ésta no cave y será rechazada en dirección posterior.
- Exploración faríngea: valoración de amígdalas, velo de paladar, úvula y amígdala lingual. La hipertrofia velopalatina es casi constante en esta patología, apareciendo en obesos y no obesos. A veces es tan marcada, que aún usando el depresor lingual y presionando con fuerza, no se puede llegar a visualizar la parte posterior de la faringe, estando ocupado el espacio del istmo de las fauces por un grueso velo de paladar que a modo de cortina cierra el paso de aire bucal, siendo difícil de ver la úvula que suele ser hipertrófica, muy larga y contacta con la lengua.
En la génesis tanto de la roncopatía como del SAOS, el velo del paladar tiene una importancia extraordinaria como ya ha quedado expuesto. Estos pacientes presentan generalmente un velo grueso y largo, si es delgado es flácido. El velo más característico del SAOS es el grueso, con aumento de volumen. En la roncopatía simple el velo característico es hipotónico o flácido. En la exploración del velo se han de precisar sus características anatómicas y funcionales, pues en el 90% de los casos presentan alteraciones más o menos importantes del mismo. A este respecto diversos autores han realizado clasificaciones de los diversos tipos de paladares. Así Ikematsu describe 16 tipos diferentes. Quesada los resume en estos tipos:
§ Paladares gruesos y cortos, con cierto edema que deja entrever una faringe relativamente estrecha.
§ Paladares tipo Webbed, en donde lo más característico es la abundancia de mucosa del paladar posterior.
§ Paladares gruesos, pletóricos y prolapsados.
§ Paladares gruesos, pletóricos, flogísticos y con úvulas largas.
§ Paladares gruesos, pletóricos y prolapsados junto a macroglosia más o menos importante.
- Las paredes faríngeas han de ser examinadas en busca de tejido excesivo o redundante, protrusiones en pared posterior por aumento de los cuerpos vertebrales de la columna cervical. Las paredes laterales pueden tener una masa submucosa excesiva o mostrar hipertrofia de los músculos.
- Laringoscopia indirecta o fibroendoscopia laríngea, visualiza el tamaño de la base de la lengua y su amígdala lingual y el estado de las estructuras hipofaríngeas y laríngeas, así como su movilidad. Funjita aconseja realizar laringoscopia indirecta, indicando que una fácil visualización de las cuerdas vocales en esta exploración es un indicador de éxito ante un tratamiento quirúrgico del SAOS.
LABORATORIO.
Se utiliza en la identificación de posibles factores etiológicos hormonales y en la evaluación de las repercusiones hematológicas del cuadro. En este sentido se solicita:
- Analítica básica: hemograma completo, ionograma, función renal y hepática, colesterol y triglicéridos. La policitemia, producida por la hipoxia nocturna es un índice de la gravedad del proceso.
- Perfil tiroideo, para descartar un posible hipotiroidismo.
ESTUDIO BÁSICO FUNCIONAL RESPIRATORIO.
- Rx de tórax.
- Espiro/inspirometría, valores de ventilación voluntaria máxima.
- Saturación por oximetría de pulso en reposo.
- Gasometría arterial si existe alteración ventilatoria o sospecha de hipoventilación.
 RADIOLOGIA.
RADIOLOGIA.
· Cefalometría.
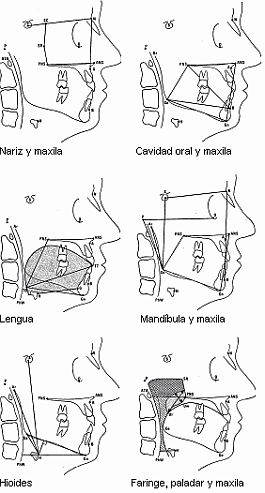
La radiología cefalométrica es una técnica sencilla y muy económica, que permite en la mitad de los casos valorar el tamaño y la posición del paladar blando, úvula y lengua, la relación entre ambos maxilares, la posición del hioides con relación al plano mandibular, así como la determinación volumétrica del espacio aéreo posterior. Esto la hace ser una ayuda importante para la selección de candidatos al tratamiento quirúrgico, si bien existen pacientes con espacio aéreo posterior reducido que no presentan colapso hipofaringeo, por lo que no debe utilizarse como un parámetro aislado de selección de pacientes. Se realiza una telerradiografía de perfil del cráneo y cervical con paciente en bipedestación, sentado o tumbado, los dientes en oposición suave y la cabeza en posición neutra con la mirada paralela al suelo, aprovechando el final de la inspiración o de la espiración (en apnea). Se valora tanto la porción esquelética como las partes blandas y se estudian los ángulos faciales, la posición el hueso hioides y el PAS:
- Ángulo formado por la espina nasal, el nasión y submentón, normal de 0 a 4º, está aumentado en la retrognatia.
- Ángulo formado por el centro de la silla turca, nasión y submentón, normal de 76 a 84º, está disminuido en la retrognatia.
- Ángulo formado por el nasión con el centro de la silla turca y la espina nasal. Normal de 76 a 88º.
- Ángulo formado entre la línea que une el Gnation con el Gonión y el nasion con el centro de la silla turca. Normal de 30 a 40º y está aumentado en la retrognatia.
· TAC.
Se puede obtener con él una excelente visualización de las VAS y de las estructuras que la rodean.
Con el TAC convencional se requieren entre 2 y 5 segundos para realizar cada corte y se necesitan 8 scans de 10 mm de espesor para valorar toda la vía aérea superior. Con el TAC ultrarrápido se ha reducido el tiempo de exploración y de radiación obteniéndose cortes 1 ó 1,5 mm, esto permite reproducir condiciones fisiológicas en tiempo real y valorar el comportamiento dinámico de la vía aérea durante el sueño. De esta forma se puede determinar el área mínima de sección de la nasofaringe, orofaringe e hipofaringe. Hapokin fue el primero en determinar con esta técnica una relación entre el grado de estrechamiento de la vía aérea durante el sueño y la gravedad del cuadro de roncopatía.
Especial interés tiene para la valoración prequirúrgica de la macroglosia.
Habitualmente es una exploración que no se realiza pues tiene el inconveniente del coste, la radiación y la dificultad para monitorizar el sueño en la sala de rayos, ahora bien es una técnica de imagen que puede detectar claramente las regiones que se colapsan durante el sueño.
 · Resonancia nuclear magnética.
· Resonancia nuclear magnética.
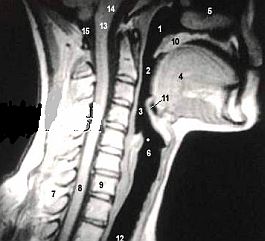
Constituye un método de diagnostico por imagen todavía más preciso que el TAC ya que permite estudiar mejor la morfología de las VAS al aportar un mayor contraste tisular e imágenes en múltiples planos sin exposición a radiaciones ionizantes. Permite además estudiar la morfología y volumetría de las VAS de forma dinámica al captar imágenes durante diferentes momentos de ciclos respiratorios consecutivos, lo que es importantísimo teniendo en cuenta que las alteraciones morfológicas faríngeas obstructivas son con frecuencia procesos transitorios, dinámicos, cambiantes y sólo identificables en ciertos momentos del ciclo respiratorio y que fuera de esos momentos pasan inadvertidas. Constituye por tanto un método excelente para detectar el lugar o lugares de obstrucción de la luz faríngea y tiene la ventaja de no radiar.
Se realiza con el paciente en decúbito dorsal, con oclusión dentaria y sin deglución. Al igual que el TAC se ha de orientar al radiólogo para obtener mediciones a nivel del borde inferior del velo, de la base de la lengua y del hueso hioides.
Informa mejor que cualquier otra imagen del grosor de las paredes de las VAS, de los músculos, así como la cantidad y localización de los depósitos grasos existentes en torno a los segmentos colapsables de la VAS en estas patologías.
Permite hacer un perfecto análisis cefalométrico con la imagen del corte sagital medio: se ha de analizar el velo del paladar y el aparato hioideo-lingual. Se ha de medir el grado de verticalización de la lengua, la posición del hueso hioides, la silueta de la orofaringe, la de la cavidad bucal y la de la lengua.
Como desventajas presenta: largo tiempo de la exploración y alto coste económico. Lo ideal es realizarla durante el sueño momento en que determinaría mejor el lugar y grado de la obstrucción faríngea, para ello el sueño suele ser inducido, o ayudado, farmacológicamente.
Todas estas exploraciones y técnicas de imagen, fibroscopia, cefalometría, TAC y RM tienen el gran handicap de que si se realizan con el paciente despierto no son claramente predectivas e idóneas par la selección de pacientes candidatos a la cirugía. Las zonas de obstrucción no son iguales en el paciente despierti y diormido, por lo que es posible que las zonas de colapso encontradas en la exploración del paciente despierto no se correpondan con las del sueño.
Las siguiente ténicas que exponemos, somnofluoroscopia y la videofibrosomnoscopia durante el sueño, son técnicas útiles para la detección preoperatoria de la zona de colapso faríngeo, si bien no son para utilizar en la práctica clínica habitual.
 VIDEOFIBROSOMNOSCOPIA.
VIDEOFIBROSOMNOSCOPIA.
Prueba también conocida como endoscopia con sueño inducido por fármacos, en inglés Drug induced sleep andoscopy.
La exploración endoscópica de las VAS del paciente durante el sueño sería un método exploratorio de mucha fiabilidad, pero tiene tantas dificultades que resulta impracticable. Es por ello que en 1991 Croft y Pringle diseñaron la endocopia con sueño inducido por fármacos, técnica que consiste en la inducción farmacológica del sueño para poder ver, con la ayuda de un fibroscopio y un equipo de video, lo que sucede en las VAS cuando el paciente está durmiendo, permitiendo determinar donde está la zona de obstrucción en el momento en que se produce la apnea en condiciones similares al sueño natural, asi como la morfología anteroposterior o circular del colapso. El sueño inducido farmacológicamente permite que los pacientes puedan tolerar la exploración fibroendocópica sin despertarse, se puede realizar la exploración incluso con dispositivos intraorales colocados y en un horario cómodo.
Croft y Pringle utilizaron como inductor del sueño el midazolan, hoy se utiliza el propofol. La realización de la prueba exige unas normas de seguridad: el lugar utilizado para su realización debe de estar equipado con medios de reanimación y con un equipo de monitorización completo por lo que nosotros aconsejamos realizar esta exploración en quirófano, encargándose de la sedación y monitorización del paciente un anestesista. Se ha de tener en cuenta que estos pacientes, algunos de ellos con un SOAS severo, tienen un importante potencial de riesgo y asocian una vía aérea de intubación difícil.
Durante la exploración, además de la simple observación, se pueden realizar maniobras de avance mandibular y colocación en decúbito lateral para ver el comportamiento de la obstrucción. Los resultados comunicados coinciden en que en la mayoría de los casos se produce una obstrucción multinivel, coincidiendo igualmente en los porcentajes en cuanto a las zonas de colapso. Así, en el 90% de los casos la obstrucción se produce en el velo del paladar, 38% en la base de la lengua, 38% en paredes laterales de la faringe y el 9% en la epiglotis. En general se observa que a mayor gravedad de la apnea existen más zonas de colapso, si bien pueden observasos SOAS leves con múltiplez zonas y SOAS graves con una sóla zona de colapso. La prueba ha sido criticada al producir un sueño inducido y no ser una técnica de registro continuo durante toda la noche.
Con los hallazgos obtenidos de esta prueba se han publicado diferentes clasificaciones: Pringle 1993, Camiller 1995, Vicini 2007, Kezirian 2011, Bachar 2012, Gillespie 2013. Exponemos la de Pringle:
Grado 1: ronquido simple.
Grado 2: obstrución sólo en velo del paladar.
Grado 3: obstrucción en velo del paladar + obstrucción intermitente sólo en inspiración en hipofaringe.
Grado 4: obstrucción en velo del paladar + colapso completo en todo el ciclo respiratorio en hipofarinte.
Grado 5: colapso hipofaríngeo, generalmente por desplazamiento anteroposterior de la lengua.
La prueba resulta util para el diagnóstico de los trastornos respiratorios producidos durante el sueño, y si bien no valora la gravedad del trastorno, si que aporta datos de las VAS que ayudan a tomar decisiones terapéuticas, especialmente las quirúrgicas.
Estaria indicada la realización de esta prueba en estas situaciones:
- Pacientes con SOAS moderado o severo. sin obesidad mórbida, que no toleren el CPAP y en los que se plantea una posibilidad de tratamiento quirúrgico.
- Paciente con SOAS leve o roncopatia simple en los que se plantea tratamiento quirúrgico.
- Pacientes en los que ha fracasado el tratamiento quirúrgico.
- Niños con SOAS residual tras Adenomaigdalectomía.
Esta prueba presenta ontraindicaciones en:
- Alergía a los componenetes del propofol o del midazolan.
- Riesgo quirúrgico elevado: ASA > 3.
Se ha argumentado en contra de la fiabilidad de la prueba que al inducir el sueño mediante el uso de fármacos, se produce una mayor relajación de la musculatura faríngea que durante el sueño natural, asi como una anulación de los reflejos naturales de las VAS. El tiempo de la exploración es corto, por lo que la prueba no tiene en cuenta la variabilidad que los episodios respiratorios pueden experimentar a lo largo de toda una noche. Se trata de una prueba subjetiva cuya valoración depende de la interpretación de un explorador. Contradiciendo estos argumentos, hay varios estudios comparativos del sueño natural y el inducido por fármacos que demuestran como este último es similar al natural en la fase NREM, dando validez a esta prueba.
Por lo que respecta a la fiabilidad de la prueba exiten controversias entre los diferentes autores que han estudiado este parámetro, especialmente cuando se trata de roncopatía simple, al boservar que el propofol puede inducir cambios en las características del ronquido: en algunos casos no produce ronquido en roncadores y en otros casos produce ronquido en no roncadores.
La utilidad práctia de esta pueba reside en que tras su realización se modifican en muchos pacientes las opciones de tratamiento a realizar, especialmente los quirúrgicos, ya que permite seleccionar mejor los candidatos a la cirugía y mejorar la indicación de la técnica quirúrgica a realizar.
REFLEXIÓN ACÚSTICA.
Técnica relativamente nueva, utilizada inicialmente para medir áreas de sección traqueal. No es invasiva, no emite radiaciones y es barata. Consiste en la emisión de ondas sonoras a través del tracto respiratorio, de forma que en aquellos segmentos en que existe un cambio en su área de sección los sonidos emitidos se reflejan parcialmente y su intensidad es recogida por un micrófono situado en la boca. Conociendo la velocidad de la onda sonora y el tiempo que tarda en llegar la reflexión acústica se puede calcular la distancia de la boca hasta el punto de reflexión. El conocimiento de los coeficientes de reflexión permite calcular el área de sección de la vía respiratoria. No es aplicable durante el sueño. No siempre es bien tolerada.
En los pacientes con SAOS se pueden apreciar unas áreas faríngeas de reflexión significativamente menores que en los pacientes no apnéicos, existiendo una elevada relación entre la dimensión de la faringe y el número de apneas por hora.
Se ha de tener en cuenta que el área faríngea cambia significativamente con el volumen pulmonar, de tal forma que al decrecer éste el volumen residual del área faríngea diminuye un 30%, ahora bien, en los pacientes con SAOS decrece hasta más de un 50%.
La experiencia que se ha ido adquiriendo con los resultados de la cirugía, ha hecho que hoy en día se de mucha más importancia para valorar la obstrucción a las pruebas que se realizan con el paciente dormido. Así se ha comprobado que no hay una correlación entre la exploración practicada con el paciente despierto mediante imágenes, TAC y RM, y los hallazgos de la VFS, al igual que tampoco se ha observado una correlación entre el IAH y la presencia de mayor o menor grado de obstrucción.
MEDICIÓN DE PRESIONES INTRAFARÍNGEAS.
La medición de presiones diferenciales entre naso, oro e hipofaringe durante el sueño, constituye la prueba conocida como MPDS. En su día fue la técnica con más valor en la localización del nivel de obstrucción. Mediante la medición de presiones diferenciales entre diferentes segmentos de las VAS permite identificar donde sucede la obstrucción y lo hace en las circunstancias más propicias, investigando desde el interior de las VAS y con el paciente dormido. La técnica es compleja pues se han de introducir una serie de catéteres intrafaríngeos con el riesgo de que pueden moverse de su sitio durante el sueño. Dada su complejidad técnica, solo se utiliza en investigación o en protocolos asistenciales. Esta complejidad y alto coste económico hacen difícil su implantación rutinaria y cotidiana.
Lo mismo ocurre con la electromiografía de las VAS. Es una técnica que permite valorar las propiedades mecánicas de las paredes, pero presentan el grave inconveniente de su compleja realización, además, los trabajos sobre la valoración de su utilidad son escasos.
Polisomnografia.
Constituye el pilar básico para el diagnóstico. Permite identificar, cuantificar y evaluar en conjunto los estadios del sueño, así como las diferentes variables fisiológicas que se producen durante el mismo, constituyendo la prueba diagnóstica de certeza en el SAOS. Es fundamental diferenciar un paciente roncador simple de aquel que junto al ronquido presenta además apneas obstructivas. La simple observación clínica del sueño es un procedimiento diagnóstico o de despistaje poco efectivo para identificar los pacientes con trastornos en la respiración y oxigenación relacionados con el sueño. Tanto para su diagnóstico como para su cuantificación es necesario la realización de estas pruebas. Se pueden realizar cuatro tipos de estudios de sueño:
1. Nivel I o polisomnografía convencional completa. La prueba consiste en el registro simultáneo de las variables neurofisiológicas y cardiorespiratorias durante el sueño para su posterior análisis y evaluación. De esta forma se identifican las diferentes fases del sueño correlacionándolas con las alteraciones cardiorespiratorias que se puedan producir, como son apneas, hipopneas, desaturaciones de O2, cambios en el ritmo cardiaco, etc. Se monitoriza la actividad cardiorespiratoria, el flujo aéreo nasobucal, los movimientos torácicos y abdominales, la saturación transcutánea de O2, el ECG, la posición corporal y opcionalmente la presión intraesofágica. Para ello se está realizando durante el sueño un EEG, un EOG, un ECG y un EMG submentoniano, lo que exige al menos cuatro canales de registro.
Mediante la EEG, EOG y EMG se valora el sueño y sus estadios. La valoración respiratoria se puede realizar mediante la detección del flujo aéreo nasobucal con termosensores o termopares, con capnografía de respuesta rápida, o con monitores de los ruidos respiratorios. El esfuerzo respiratorio se detecta mediante bandas toracoabdominales simples o pletismografía de inductancia, que permite una medida del volumen movilizado.
Se realiza continuamente una medición de los gases arteriales, lo que permite conocer la repercusión de las apneas en los mismos. La saturación de O2 se mide mediante pulxiosimetría por técnica espectofotométrica en el ámbito digital. La presión de CO2 se detecta mediante electrodos transcutáneos y su determinación no está generalizada en estos estudios de sueño.
El registro ECG permite valorar los trastornos del ritmo durante las apneas.
El registro de los movimientos de las extremidades mediante EMG tibial es útil para el diagnostico de mioclonias y síndrome de las piernas inquietas.
El informe de sueño obtenido mediante este método debe de recoger los siguientes datos:
- Las variables que mide y por qué métodos.
- Estructura del sueño.
- Relación de la posición corporal con los eventos registrados. Así puede ocurrir que un paciente con SAOS presente un estudio normal si durante el estudio no ha adoptado la posición de decúbito supino.
- Anomalías respiratorias: apneas, hipopneas o respiración periódica. Indices, duración media, tipo y su relación con la fase del sueño.
- Oxigenación arterial inicial y descensos en relación con las apneas o hiponeas.
- Alteraciones cardíacas: ritmo en relación con los estadios del sueño y las anomalías respiratorias.
- Comentarios técnicos sobre las posibles incidencias, tolerancia, nicturia, etc.
- Juicio clínico.
Este es el método de diagnóstico más preciso, aunque también es el más laborioso, complejo y caro, ya que requiere la presencia constante de personal especializado para supervisar y atender el estudio durante toda la noche y dado la cantidad de datos que aporta su interpretación lleva tiempo, si bien hoy se dispone de interpretación computarizada. No suele ser bien tolerado por los enfermos dada la incomodidad que producen los detectores que conlleva y el medio hospitalario en que se realiza.
2. Nivel II. Los inconvenientes que plantea el nivel I han obligado a la búsqueda de alternativas diagnósticas más sencillas. El nivel II es un estudio completo pero sin vigilancia, realizándose con equipos de polisomnografia portátil en el hogar, que permiten analizar los mismos parámetros que en el estudio convencional: las variables neurofisiológicas y cardiorespiratorias habituales. Con relación al nivel I es más eficaz en relación con el costo. Puede incluso ser más preciso que el I, al realzarse en el entorno natural del paciente. El estudio se realiza de forma no supervisada lo que puede conllevar la pérdida de datos y algunos registros no válidos. El estudio se puede hacer a través de moden que alertaría a un técnico que se encuentra en el hospital si existe algún problema, de tal forma que pueda hacer una llamada telefónica para corregirlo.
3. Nivel III o poligrafía cardiorespiratoria nocturna. Son estudios parciales que se realizan a domicilio Se monitorizan solamente las variables cardiorespiratorias, registrándose el flujo aéreo nasobucal, los movimientos respiratorios toracoabdominales, la saturación trascutánea de 02, la posición corporal, el ECG y, en ocasiones, el ronquido. Al no registrarse las variables neurofisiológicas no es posible estudiar la arquitectura del sueño, la duración de sus distintas fases ni el tiempo durante el cual el enfermo ha estado dormido. Es un método más sencillo que el anterior, puede hacerse a domicilio, no requiere vigilancia y se acepta bastante bien por el enfermo. Su especificidad en la identificación del SAOS es alta y su sensibilidad es también buena, lo que ha hecho que en los últimos años se plantee como una alternativa a la polisomnografía convencional. No obstante, esta prueba tiene sus limitaciones, por lo que en ocasiones hay que recurrir a la anterior, tal es el caso de enfermos con manifestaciones clínica muy evidentes y con un estudio negativo, o cuando la respuesta al tratamiento de CPAP no es la esperada.
4. Nivel IV: pulsioximetría nocturna simple. Consiste en el registro nocturno del pulso y de la saturación arterial de O2 medida mediante un sensor espectofotométrico colocado en un dedo. Va registrando las desaturaciones que se producen en las apneas así como las oscilaciones del pulso, bradicardias-taquicardias típicas del SAOS.
En las roncopatías esta prueba ha de ser considerada como un método de despistaje con claras limitaciones diagnósticas, por lo que su indicación ante la sospecha de SAOS o en el estudio evolutivo de la enfermedad se reduce a casos muy limitados. La sensibilidad y especificidad de esta prueba para detectar un SAOS es baja, pues depende del criterio de, pudiendo pasar por alta SAOS leves o moderados. La inspección visual de la curva de saturación proporciona una excelente especificidad, al igual que sí se utilizan índices cuantitativos, como es el cálculo del número de desaturaciones > 4% por hora. Por el contrario, el análisis del porcentaje de tiempo acumulado con SO2<90% (CT90%) proporciona una elevada sensibilidad. Un CT 90%<1% prácticamente descarta la enfermedad.
La pulsioximetría puede ser por tanto de utilidad en la selección de pacientes más graves, o bien puede servir como método de discriminación cuando se utiliza de forma conjunta con un modelo de predicción clínica. Se aconseja tener una especial precaución en la valoración de esta prueba en los pacientes con EPOC o insuficiencia cardíaca, ya que estos pacientes pueden presentar desaturación arterial nocturna independientemente de que estén o no afectos de un SAOS. Tiene la ventaja de ser una técnica con una muy buena relación rentabilidad/precio, puede realizarse de forma ambulatoria y permite almacenar la información y analizarla por métodos informáticos.
Otro método propuesto es el registro de ruidos traquéales y frecuencia cardiaca: MESAM. Consiste en un equipo de registro automatizado compuesto por un micrófono instalado en el cuello y tres electrodos torácicos para el registro del pulso.
Los métodos de diagnostico simplificado aportan una mayor disponibilidad y una mejor adaptación al estudio por parte del paciente ya que permiten realizar el registro en el propio domicilio. La reducción del coste económico es un punto controvertido, ya que la utilización de un método simplificado puede conllevar la repetición innecesaria de exploraciones, debido a los falsos diagnósticos o a los fallos de registro que se producen en un estudio no supervisado. Entre las desventajas cabe citar, la menor fiabilidad y las limitaciones diagnósticas que comportan.
Además de su interés diagnóstico pretratamiento, estas pruebas tienen igualmente interés durante el tratamiento y en el postratamiento, pues son necesarias para realizar la valoración de la eficacia de mismo y para la identificación de aquellos casos en que persisten criterios de enfermedad tras la cirugía precisando de otro tipo de tratamiento.
¿ Cómo elegir que método de diagnóstico se ha de realizar? Los métodos simplificados son los adecuados para realizarlos a pacientes roncadores, con escasa clínica de SAOS, y sólo si el resultado fuese equívoco sería necesario realizar un estudio más complejo. Igualmente se podría realizar en pacientes con clínica evidente, roncadores con episodios de apneas observadas durante la noche, nicturia y somnolencia diurna. De esta forma se pueden detectar los casos más graves e indicar el tratamiento de forma precoz.
En los pacientes con una clínica de SAOS incompleta o no suficientemente convincente, sería preferible realizar de entrada un estudio convencional que despejaría las dudas sobre el diagnóstico y las necesidades de tratamiento. Igualmente en pacientes con excesiva somnolencia diurna sin otras características clínicas que sugieran un SAOS, estaría también indicado un estudio polisomnográfico convencional para descartar otras entidades tales como la narcolepsia o las mioclonias nocturnas. Tras estudios simplificados poco concluyentes o cuando el tratamiento con CPAP no resulta efectivo se ha de recurrir igualmente a la polisomnografía convencional.
Los criterios polisomnográficos habitualmente aceptados para establecer el diagnóstico de un SAOS se basan en los índices de apnea y de apnea-hipopnea, que deben de ser superiores a cinco o a diez, respectivamente, siempre y cuando se acompañen de un cuadro clínico compatible. Sin embargo, no hay siempre una buena correlación entre ellos y la gravedad de las manifestaciones clínicas. El número de desaturaciones, su profundidad y su duración permiten estimar la gravedad de un SAOS, pero sin olvidar que para evaluar adecuadamente este aspecto también hay que tener en cuenta las manifestaciones clínicas, las enfermedades coincidentes y las repercusiones laborales y sociales.
Ya hemos comentado que la valoración de la hiponeas no es uniforme entre los diferentes autores. Así se puede valorar mediante la medición flujo aéreo por termistancia considerando positiva una reducción del 50%. El mismo flujo ventilatorio puede ser medido mediante pletismografía. La valoración puede igualmente hacerse combinando la medida de las reducciones en el flujo aéreo con la medida de los descensos de saturación arterial de O2 con pulsioxímetro, considerándose positiva reducciones de al menos 4%.
Cuando un estudio poligráfico es positivo, es necesario efectuar un segundo registro nocturno. En él deben evaluarse los efectos de la CPAP y han de ajustarse los niveles mínimos de presión necesaria que ha de generar para que desaparezcan las apneas e hipopneas, los despertares subconscientes y las desaturaciones.
EVALUACIÓN CARDIOLÓGICA.
Bien con motivo de la polisomnografía, o independientemente de ella, se aconseja realizar una valoración cardiológica, especialmente recomendada en los cuadros de larga evolución para la valoración de la posible sobrecarga del ventrículo derecho.
